生物学的プロセス、機能、命名法およびサブクラスのトランスフェラーゼ
の トランスフェラーゼ 供与体として作用する基質の官能基を受容体として作用する他の官能基に転移させる原因となる酵素である。生命に欠かせない代謝プロセスのほとんどは、トランスフェラーゼ酵素を含みます.
これらの酵素によって触媒される反応の最初の観察は、アルカリホスファターゼからホスフェート基の受容体として作用するβ-ガラクトシダーゼへのホスフェート基の転移を観察したR.K.Morton博士によって1953年に文書化された。.

トランスフェラーゼ酵素の命名は、一般に、反応において官能基を受容する分子の性質、例えば、DNA−メチルトランスフェラーゼ、グルタチオン - トランスフェラーゼ、1,4 − α−グルカン6 − α−グルコシルトランスフェラーゼ、によって行われる。とりわけ.
トランスフェラーゼは、特に食品医薬品業界で、バイオテクノロジー的に重要な酵素です。それらの遺伝子は、生物の特定の活動を満たすように改変することができ、栄養上の利益を超えて、消費者の健康に直接貢献します。.
これらは腸内の有益な微生物の成長と発展を支持炭水化物の形成に関与しているとして、腸内細菌叢のためのプレバイオティクス薬は、トランスフェラーゼが豊富です.
欠陥は、構造的損傷及び破壊は細胞産物内蓄積原因プロセストランスフェラーゼ触媒、非常に多くの異なる疾患および病状は、そのような酵素に関連しています.
トランスフェラーゼの機能不全は、とりわけ、ガラクトース血症、アルツハイマー病、ハンチントン病などの疾患を引き起こす。.
索引
- 1彼らが参加する生物学的プロセス
- 2つの機能
- 3命名法
- 4サブクラス
- 4.1 EC.2.1炭素原子の移動基
- 4.2 EC.2.2アルデヒドまたはケトン基の移動
- 4.3 EC.2.3アシルトランスフェラーゼ
- 4.4 EC.2.4グリコシルトランスフェラーゼ
- 4.5 EC.2.5メチル基とは別にアルキルまたはアリール基を移動する
- 4.6 EC.2.6窒素基の移動
- 4.7 EC.2.7リン酸基を含む移動基
- 4.8 EC.2.8硫黄を含む移動基
- 4.9 EC.2.9セレンを含む移動基
- 4.10 EC.2.10モリブデンまたはタングステンのいずれかを含む移動基
- 5参考文献
彼らが参加する生物学的プロセス
トランスフェラーゼが関与する多数の代謝過程の中には、グリコシド生合成および糖の代謝一般がある。.
酵素グルコトランスフェラーゼは、赤血球の表面上の抗原AおよびBの抱合に関与している。抗原結合におけるこれらの変異は、B-トランスフェラーゼの元の構造のPro234Serアミノ酸の多型に由来する.
肝臓のグルタチオン-S-トランスフェラーゼは肝細胞の解毒に関与し、細胞質に蓄積する活性酸素種(ROS)、フリーラジカル、過酸化水素からそれらを保護するのを助けます。毒性が強い.
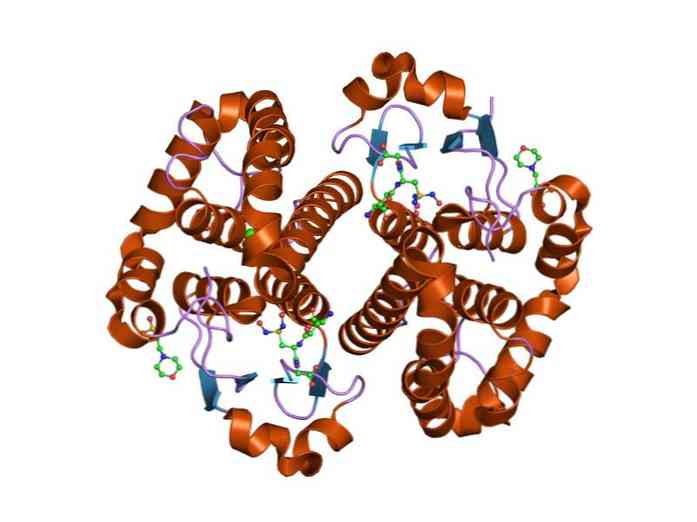
アスパラギン酸カルバモイルトランスフェラーゼは、ヌクレオチド、核酸の基本成分、および複数の細胞プロセスで使用される高エネルギー分子(例えば、ATPおよびGTPなど)の代謝におけるピリミジンの生合成を触媒する。.
トランスフェラーゼは、エピジェネティックなメカニズムによって細胞要素の合成に必要な情報をコードするDNA配列をサイレンシングすることによって、多くの生物学的プロセスの調節に直接関与しています.
ヒストンアセチルトランスフェラーゼは、アセチル-CoA分子からアセチル基を転移させることにより、ヒストン中の保存されたリジン残基をアセチル化した。このアセチル化は、ユークロマチンの発生または弛緩に関連する転写の活性化を刺激する.
ホスホトランスフェラーゼは、おそらく全ての細胞代謝の状況において、リン酸基の転移を触媒する。炭水化物のリン酸化に重要な役割を果たしています.
アミノトランスフェラーゼは、オキシ酸アミノ酸からアミノ基の可逆的転移を触媒依存性酵素のビタミンB6を媒介するアミノ酸の多くの変換の一つ.
機能
トランスフェラーゼは、以下に示される反応を満たす化学基の移動を触媒する。以下の式において、文字「X」は官能基「Y」のドナー分子を表し、そして「Z」はアクセプターとして作用する。.
X-Y + Z = X + Y-Z
これらは、その組成中に強い電気陰性および求核元素を含む酵素です。これらの要素は酵素の移動容量に責任があります.
トランスフェラーゼによって動員される基は、一般に、とりわけアルデヒドおよびケトン残基、アシル、グルコシル、アルキル、窒素および窒素に富む基、リン、硫黄含有基である。.
命名法
トランスフェラーゼの分類は、1961年に酵素委員会によって提案された酵素の分類のための一般的な規則に従います。委員会によると、各酵素はその分類のための数値コードを受け取ります.
コード内の番号の位置は、分類内の各部門またはカテゴリを示し、これらの番号の前には文字 "EC"が付きます。.
ランキングトランスフェラーゼ最初の番号は、酵素クラスを表し、2番目の数字は転送タイプのグループを象徴し、3番目の数字は、それらが作用している基板を指し.
トランスフェラーゼのクラスの命名は、 EC.2. それは10のサブクラスを持っているので、酵素はからのコードで見つけられます EC.2.1 まで EC.2.10. サブクラスの各表示は、主に酵素を伝達するタイプグループに従って行われます。.
サブクラス
トランスフェラーゼファミリー内の10種類の酵素は次のとおりです。
EC.2.1炭素原子の移動基
それらは単一の炭素を含む基を移動させる。例えば、メチルトランスフェラーゼはメチル基(CH 3)をDNAの窒素含有塩基に転移させる。このグループの酵素は直接遺伝子の翻訳を調節します.
EC.2.2アルデヒドまたはケトン基の移動
それらは、受容体基として糖を有するアルデヒド基およびケトン基を動員する。カルバミルトランスフェラーゼはピリミジン類の調節と合成の機構を表す.
EC.2.3アシルトランスフェラーゼ
これらの酵素はアシル基をアミノ酸誘導体に転移する。ペプチジルトランスフェラーゼは翻訳過程で隣接アミノ酸間のペプチド結合の必須形成を行う.
EC.2.4グリコシルトランスフェラーゼ
それらはドナー基としてリン酸糖基を用いてグリコシド結合の形成を触媒する。すべての生物は、糖脂質や糖タンパク質の合成に関与しているので、グリコシルトランスフェラーゼのDNA配列を提示します。.
EC.2.5メチル基とは別にアルキルまたはアリール基を移動させる
それらは、例えばアルキル基またはアリール基(CH 3以外)をジメチル基として動員する。それらの中には、グルタチオントランスフェラーゼがあり、それは上記の通りである。.
EC.2.6窒素基の移動
このクラスの酵素は、-NH 2および-NHなどの窒素基を移動させる。これらの酵素の中には、アミノトランスフェラーゼとトランスアミナーゼがあります。.
EC.2.7リン酸基を含む移動基
それらは基質のリン酸化を触媒する。一般に、これらのリン酸化の基質は糖や他の酵素です。ホスホトランスフェラーゼは糖を同時にリン酸化することによって糖を細胞内部に輸送する.
EC.2.8硫黄を含む移動基
それらは、それらの構造中の硫黄含有基の移動を触媒することを特徴とする。コエンザイムAトランスフェラーゼはこのサブクラスに属します.
EC.2.9セレンを含む移動基
それらは一般にセレノトランスフェラーゼとして知られている。これらはL-セリル基を動員してRNAを移動させる.
EC.2.10モリブデンまたはタングステンのいずれかを含む基を移動する
この群のトランスフェラーゼは、モリブデンまたはタングステンを含む基をアクセプターとしてスルフィド基を有する分子に動員する。.
参考文献
- アルファロ、J. A.、鄭、R. B.、Perssonの、M.、レッツ、J. A.、Polakowski、R.、白、Y.、...&エバンス、S. V.(2008)。特定のグリコシルトランスフェラーゼを介しABO(H)血液型AおよびBは、基板コンフォメーション変化を認識する。生物化学のジャーナル、283(15)、10097から10108.
- Aranda Moratalla、J.(2015)。 DNA‐メチルトランスフェラーゼの計算研究DNAメチル化のエピジェネティックなメカニズムの分析(Thesis-Doctoral、バレンシア大学 - スペイン).
- Armstrong、R.N.(1997)。グルタチオントランスフェラーゼの構造、触媒機構、および進化毒物学における化学研究、10(1)、2-18.
- Aznar Cano、E.(2014)。表現型および遺伝子型法による「Helicobacter pylori」のファージ研究(博士論文、Universidad Complutense de Madrid)
- Boyce、S.、&Tipton、K. F.(2001)。酵素の分類と命名eLS.
- Bresnick、E.、&Mossé、H.(1966)。ラット肝臓のアスパラギン酸カルバモイルトランスフェラーゼBiochemical Journal、101(1)、63.
- ガニョン、M. S.、レッグ、M. S.、Polakowski、R.、レッツ、J. A.、Perssonの、M.、リン、S.、...&Borisova、S. N.(2018)。保存された残基Arg188およびAsp302は、人間のABO(H)血液型AとBの糖転移酵素で触媒作用と活性部位の組織のために重要です。糖鎖生物学、28(8)、624から636まで
- Grimes、W.J.(1970)。正常細胞と形質転換細胞におけるシアル酸トランスフェラーゼとシアル酸濃度Biochemistry、9(26)、5083-5092.
- Grimes、W.J.(1970)。正常細胞と形質転換細胞におけるシアル酸トランスフェラーゼとシアル酸濃度Biochemistry、9(26)、5083-5092.
- Hayes、J. D.、Flanagan、J. U.、&Jowsey、I. R.(2005)。グルタチオントランスフェラーゼアンヌ。 Pharmacol。 Toxicol。、45、51-88.
- Hersh、L. B.、&Jencks、W. P.(1967)。補酵素Aトランスフェラーゼの速度論と交換反応Journal of Biological Chemistry、242(15)、3468-3480
- Jencks、W. P.(1973)。 11コエンザイムAトランスフェラーゼ。酵素(Vol。9、p。483-496)。学術プレス.
- Lairson、L.L.、Henrissat、B.、Davies、G.J.&Withers、S.G.(2008)。グリコシルトランスフェラーゼ:構造、機能、およびメカニズム生化学の年次レビュー、77
- Lairson、L.L.、Henrissat、B.、Davies、G.J.&Withers、S.G.(2008)。グリコシルトランスフェラーゼ:構造、機能、およびメカニズム生化学の年次レビュー、77.
- Lambalot、R.H.、Gehring、A.M.、Flugel、R.S.、Zuber、P.、LaCelle、M.、Mahahiel、M.A。、...&Walsh、C.T.(1996)。新しい酵素スーパーファミリーのホスホパンテテイニルトランスフェラーゼChemistry&biology、3(11)、923-936
- Mallard、C.、Tolcos、M.、Leditschke、J.、Campbell、P.、およびRees、S.(1999)。 SIDS乳児の脳幹におけるコリンアセチルトランスフェラーゼ免疫反応性の低下、ムスカリンm 2受容体免疫反応性の低下神経病理学と実験神経学、58(3)、255-264
- Mannervik、B。(1985)。グルタチオントランスフェラーゼのアイソザイム酵素学および分子生物学の関連分野における進歩、57、357-417
- MEHTA、P. K.、HALE、T. I.、およびCHRISTEN、P.(1993)。アミノトランスフェラーゼ相同性の証明と進化的サブグループへの分割European Journal of Biochemistry、214(2)、549-561
- E.、Staehelin、T.、Celma、M.L。&Vazquez、D。(1969年1月)。リボソームのペプチジルトランスフェラーゼ活性量的生物学に関するコールドスプリングハーバーシンポジウム(Vol。34、pp。357-368)。コールドスプリングハーバーラボラトリープレス.
- Montes、C.P.(2014)。食品中の酵素は?食用の生化学大学ジャーナルUNAM、15、12.
- Morton、R. K.(1953)。加水分解酵素のトランスフェラーゼ活性ネイチャー、172(4367)、65.
- Negishi、M.、Pedersen、L.G.、Petrotchenko、E.、Shevtsov、S.、Gorokhov、A.、Kakuta、Y.&Pedersen、L.C.(2001)。スルホトランスフェラーゼの構造と機能生化学と生物物理学のアーカイブ、390(2)、149-157
- 国際生化学分子生物学連合の命名委員会(NC-IUBMB)。 (2019)。 qmul.ac.ukから取得
- Rej、R.(1989)。疾患におけるアミノトランスフェラーゼ臨床検査医学、9(4)、667-687.
- Xu、D.、Song、D.、Pedersen、L.C.&Liu、J.(2007)。ヘパラン硫酸2 ‐ O‐スルホトランスフェラーゼとコンドロイチン硫酸2 ‐ O‐スルホトランスフェラーゼの突然変異研究Journal of Biological Chemistry、282(11)、8356-8367


