無水の性質、それらの形成方法、命名法、用途
の 無水物 それらは、水の放出を介して2つの分子の結合から生じる化合物です。したがって、それは最初の物質の脱水として見ることができます。正確ではありませんが.
有機および無機化学ではそれらについて言及されており、両方の分野でそれらの理解はかなりの程度異なる。例えば、無機化学では、前者が水と反応して後者を形成するので、塩基性および酸性酸化物はそれぞれそれらの水酸化物および酸の無水物と見なされる。.

ここで、用語「無水」と「無水」の間に混乱が生じる可能性があります。一般に、無水とは、その化学的性質に変化を生じることなく脱水された化合物をいう(反応なし)。一方、無水物では、分子構造に反映された化学変化があります。.
水酸化物および酸をそれらの対応する酸化物(または無水物)と比較すると、反応があることが観察されるであろう。対照的に、いくつかの酸化物または塩は水和し、水を失い、そして同じ化合物のままであり得る。しかし、水なしでは、つまり、無水.
一方、有機化学では、無水物が意味するものは最初の定義です。例えば、最も知られている無水物の一つはカルボン酸の誘導体です(上の画像)。これらは酸素原子による二つのアシル基の結合(-RCO)からなる。.
その一般構造において、それはRで示される。1 アシル基の場合、およびR2 第二アシル基のため。 Rだから1 とR2 それらは異なり、それらは異なるカルボン酸に由来し、そしてそれはそれから非対称酸無水物である。両方のR置換基(それらが芳香族であるかどうかにかかわらず)が同じである場合、我々はこの場合、対称酸無水物について話している。.
2つのカルボン酸を結合させて無水物を形成するときに、他の化合物と同様に、水が形成されてもされなくてもよい。すべてが前記酸の構造に依存します.
索引
- 1無水物の性質
- 1.1化学反応
- 2無水物はどのように形成されますか?
- 2.1環状無水物
- 3命名法
- 4アプリケーション
- 4.1有機無水物
- 5例
- 5.1無水コハク酸
- 5.2無水グルタル酸
- 6参考文献
無水物の性質
無水物の特性はあなたが参照しているものに依存します。ほとんどの人が水と反応するという共通点があります。しかしながら、無機のいわゆる塩基性無水物については、実際にはそれらのいくつかは水(MgO)にさえ不溶性でさえあるので、この記述はカルボン酸の無水物に焦点を合わせるであろう。.
融点と沸点は(RCO)の分子構造と分子間相互作用にある2あるいは、これがこれらの有機化合物の一般的な化学式です。.
分子量が(RCO)の場合2またはそれは低いです、それはおそらく室温と圧力で無色の液体です。例えば、無水酢酸(または無水エタノール)、(CH3CO)2あるいは、それは液体であり、工業的に非常に重要なものであり、その生産は非常に広大である.
無水酢酸と水との反応は以下の化学式で表される。
(CH3CO)2O + H2O => 2CH3COOH
水分子が添加されると、2分子の酢酸が放出されることに留意されたい。しかしながら、逆反応は酢酸に対しては起こり得ない。
2CH3COOH =>(CH3CO)2O + H2○(起こらない)
別の合成ルートに頼る必要があります。一方、ジカルボン酸は加熱することで可能になります。しかし、それは次のセクションで説明されます.
化学反応
加水分解
無水物の最も単純な反応の1つはそれらの加水分解であり、これは無水酢酸について示されたばかりである。この例に加えて、硫酸無水物があります。
H2S2○7 + H2○ <=> 2H2そう4
無機酸無水物があります。 Hに注意してください2S2○7 (二硫酸とも呼ばれる)反応自体は可逆的なので、Hを加熱する2そう4 濃縮物はその無水物の形成をもたらす。一方、それがHの希薄溶液であるならば2そう4, SOが解放されました3, 無水硫酸.
エステル化
酸無水物はアルコールと、媒体中のピリジンと反応してエステルおよびカルボン酸を生成する。たとえば、無水酢酸とエタノールの反応は次のように考えられます。
(CH3CO)2O + CH3CH2OH => CH3CO2CH2CH3 + CH3COOH
こうしてエチルエステルエタノエート、CHを形成する。3CO2CH2CH3, とエタン酸(酢酸).
実際に起こることは、アシル基によるヒドロキシル基の水素の置換である。
R1-OH => R1-OCOR2
(CHの場合3CO)2または、あなたのアシル基は-COCHです3. したがって、OH基はアシル化を受けていると言われている。しかしながら、アシル化とエステル化は交換可能な概念ではない。アシル化は、Friedel-Craftsアシル化として知られる芳香環中で直接起こり得る。.
従って、酸無水物の存在下でのアルコールはアシル化によりエステル化される。.
他方、2つのアシル基のうちの一方のみがアルコールと反応し、他方は水素と一緒に留まりカルボン酸を形成する。 (CHの場合は3CO)2または、それはエタノール酸です.
アミド化
酸無水物はアンモニアまたはアミン(一級および二級)と反応してアミドを生成する。反応は今述べたエステル化と非常に類似しているが、ROHはアミンで置き換えられている。例えば、第二級アミン、R2NH.
また、(CH間の反応3CO)2Oとジエチルアミン、Et2NH:
(CH3CO)2O + 2Et2NH => CH3CONEt2 + CH3COO-+NH2Et2
そしてジエチルアセトアミド、CHが形成される3CONEt2, カルボン酸アンモニウム塩、CH3COO-+NH2Et2.
この方程式は理解するのが少し難しいように思われるかもしれませんが、グループ-COCHがどのようになるかを観察するのに十分です。3 EtのHを置き換える2アミドを形成するNH:
Et2NH => Et2NCOCH3
アミド化以上に、反応は依然としてアシル化である。すべてがその言葉にまとめられています。今度は、アミンはアシル化を受け、アルコールは受けません.
無水物はどのように形成されますか?
無機無水物は、元素を酸素と反応させることによって形成される。したがって、元素が金属の場合、塩基性金属酸化物または無水物が形成される。そしてそれが非金属であれば、非金属酸化物または酸無水物が形成される。.
有機無水物の場合、反応は異なります。 2つのカルボン酸は直接結合して水を放出して酸無水物を形成することはできない。まだ言及されていない化合物の参加が必要です:塩化アシル、RCOCl.
カルボン酸は塩化アシルと反応して、それぞれ無水物と塩化水素を生成する。
R1COCl + R2COOH =>(R1CO)O(COR)2)+ HCl
CH3COCl + CH3COOH =>(CH3CO)2O + HCl
A CH3 アセチル基、CHから来る3CO-と他のものはすでに酢酸中に存在しています。カルボン酸と同様に特定の塩化アシルを選択すると、対称または非対称の酸無水物を合成することができる。.
環状無水物
塩化アシルを必要とする他のカルボン酸とは異なり、ジカルボン酸はそれらの対応する無水物中で縮合させることができる。このためには、Hの放出を促進するためにそれらを加熱する必要があります。2例えば、フタル酸から無水フタル酸の生成が示されている。.

五角形の環がどのようにして完成し、そして両方の基C = Oを結合する酸素もその一部であることに注意してください。これは環状無水物です。また、無水フタル酸は対称無水物であることが分かる。1 Rとして2 それらは同一です:芳香環.
全てのジカルボン酸がそれらの無水物を形成することができるわけではない。なぜなら、それらのCOOH基が広く分離されている場合、それらはますます大きな環を完成することを強いられるからである。形成され得る最大の環は六角形のものであり、反応が起こらないことよりも大きい。.
命名法
無水物はどのように命名されていますか?酸化物に関連した無機物を除けば、これまで説明した有機酸無水物の名前はRの正体に依存する。1 とR2;つまり、そのアシル基の.
2つのRが同じである場合、それぞれのカルボン酸の名称において「酸」という用語を「酸無水物」に置き換えることで十分である。そして反対に、2つのRが異なる場合、それらはアルファベット順に命名されます。それゆえ、それを何と呼ぶべきかを知るためには、それが最初にそれが対称的または非対称的酸無水物であるかどうかを見ることが必要である。.
(CH3CO)2または、Rから対称です。1= R2 = CH3. 酢酸またはエタン酸の誘導体なので、その名前は、前述の説明のとおり、無水酢酸またはエタン酸です。今述べた無水フタル酸についても同様である。.
次の無水物があるとします。
CH3CO(O)COCH2CH2CH2CH2CH2CH3
左側のアセチル基は酢酸に由来し、右側のものはヘプタン酸に由来する。この無水物に名前をつけるには、アルファベット順にRグループに名前を付けなければなりません。だから、その名前は次のとおりです。ヘプタン酸無水物.
アプリケーション
無機無水物は、材料、セラミック、触媒、セメント、電極、肥料などの合成および配合から、その数千の鉄およびアルミニウム鉱物、および二酸化物による地殻の被覆まで、無限の用途を有する。生物によって排出される炭素の量.
それらは出発の源、すなわち無機合成に使用される多くの化合物が由来する点を表す。最も重要な無水物の一つは二酸化炭素、COです。2. それは、水と共に、光合成に不可欠です。産業レベルでは、3 それは被告がそれから硫酸を得るのでそれは最も重要です.
おそらく、より多くの用途を持ちそして(寿命がある限り)持っている無水物は、リン酸からのものである:ATPとしてよりよく知られている、アデノシン三リン酸は、DNAに存在し、そして代謝の「エネルギー通貨」.
有機無水物
酸無水物は、アルコール、エステル、アミンのいずれかにアシル化することによって反応し、アミドまたは芳香環を生じる。.
これらの化合物はそれぞれ数百万種類あり、無水物を調製するためのカルボン酸の選択肢は数十万種類あります。したがって、合成の可能性は劇的に成長します.
したがって、主な用途の1つは、その構造の原子または基の1つを置換して、アシル基を化合物に組み込むことである。.
各無水物は別々にそれ自身の用途を有するが、一般的に言えばそれらは全て同様の方法で反応する。このため、これらの種類の化合物は、ポリマー構造を変更して新しいポリマーを作成するために使用されます。すなわち、コポリマー、樹脂、コーティングなど。.
例えば、無水酢酸はセルロースの全てのOH基をアセチル化するために使用される(下の画像)。これにより、OHの各Hはアセチル基COCH 3によって置換される。3.
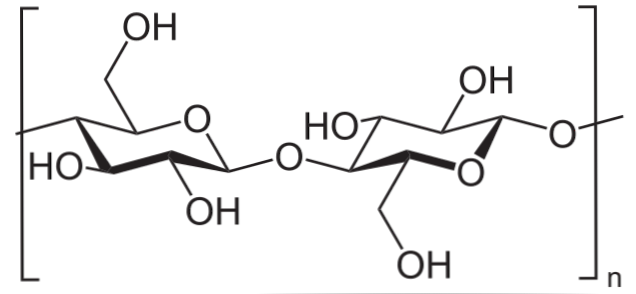
このようにしてセルロースアセテートポリマーが得られる。同じ反応は、NH基を有する他のポリマー構造でもスケッチすることができる。2, アシル化も受けやすい.
これらのアシル化反応はアスピリン(酸)のような薬物の合成にも有用です。 アセチルサリチル酸).
例
有機無水物の他のいくつかの例が完成することが示されている。それらについては言及されていないが、酸素原子はイオウで置換することができ、イオウ、さらには無水リンを与える。.
-C6H5CO(O)COC6H5:無水安息香酸。グループC6H5 ベンゼン環を表す。その加水分解は2つの安息香酸を作り出す.
-HCO(O)COH:無水ギ酸。その加水分解は2つのギ酸を作り出す.
- C6H5CO(O)COCH2CH3安息香酸プロパン酸無水物。その加水分解は安息香酸とプロパン酸を生成する.
-C6H11CO(O)COC6H11:シクロヘキサンカルボン酸無水物。芳香環とは異なり、これらは二重結合なしで飽和しています.
-CH3CH2CH2CO(O)COCH2CH3:無水ブタン酸プロパン酸.
無水コハク酸

ここには、コハク酸、ジカルボン酸から誘導されたもう一つの環状化合物があります。 3つの酸素原子がこの種の化合物の化学的性質をどのように裏切っているかに注意してください。.
無水マレイン酸は無水コハク酸に非常に似ていますが、五角形のベースを形成する炭素間に二重結合があるという違いがあります。.
無水グルタル酸
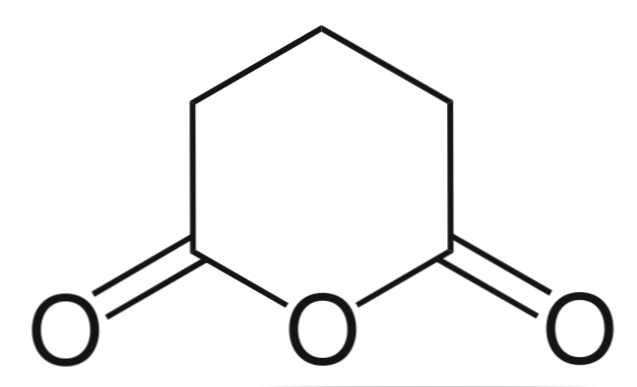
そして最後に、グルタル酸の無水物が示されています。これは六角形の環からなることにより構造的に他のすべてのものと区別される。繰り返しますが、3つの酸素原子が構造の中で際立っています.
より複雑な他の無水物は、互いに非常に近い3つの酸素原子によって常に証明されます。.
参考文献
- ブリタニカ百科事典の編集者。 (2019)。無水物Encryclopaedia Britannica。取得元:britannica.com
- Helmenstine、Anne Marie、Ph.D. (2019年1月8日)化学における酸無水物の定義以下から取得しました:thoughtco.com
- 化学ライブラリテキスト。 (S.F.)。無水物取得元:chem.libretexts.org
- Graham Solomons T.W.、Craig B. Fryhle。 (2011)。有機化学アミン(10番目 版。)。ワイリープラス.
- Carey F.(2008)。有機化学(第6版)。マックグローヒル.
- ホワイト、デイビス、ペック、スタンレー。 (2008)。化学(第8版)。 CENGAGEラーニング.
- モリソンとボイド。 (1987)有機化学(第5版)。アディソン - ウェズリーイベロアメリカーナ.
- ウィキペディア(2019)。有機酸無水物取得元:en.wikipedia.org


