周期律表と実施例における原子量の変化
の 原子量 元素のモル質量とその密度の関係を示す相対値です。そのため、この体積は元素の密度に依存し、密度は相および原子がこの原子内にどのように配置されているかにも依存します。.
そのため、Z元素の原子体積は、室温(液体、固体、気体)で現れるものとは異なる別の相、または特定の化合物の一部である場合とは異なります。従って、化合物ZA中のZの原子体積は、化合物ZB中のZのそれとは異なる。.

なんで?それを理解するためには、例えば大理石と原子を比較する必要があります。大理石は、優れた画像の青みがかったものと同様に、その鮮やかな表面のおかげで観察されるそれらの物質的な境界を非常によく定義しています。対照的に、原子の境界は拡散していますが、それらは遠方の球形と見なすことができます.
したがって、原子境界を超えた点を決定するのは電子を見つける零確率であり、この点は、考慮している原子の周りでいくつの隣接原子が相互作用するかに応じて、原子核により遠くまたは近くなる。.
索引
- 1原子体積と半径
- 2追加式
- 3周期表における原子体積の変化?
- 3.1遷移金属の原子量
- 4例
- 4.1例1
- 4.2例2
- 5参考文献
原子体積と半径
H分子内の2つのH原子を相互作用させることによって2, それらの核の位置とそれらの間の距離(核間距離)が定義される。両方の原子が球形の場合、半径は核と拡散境界の間の距離です。
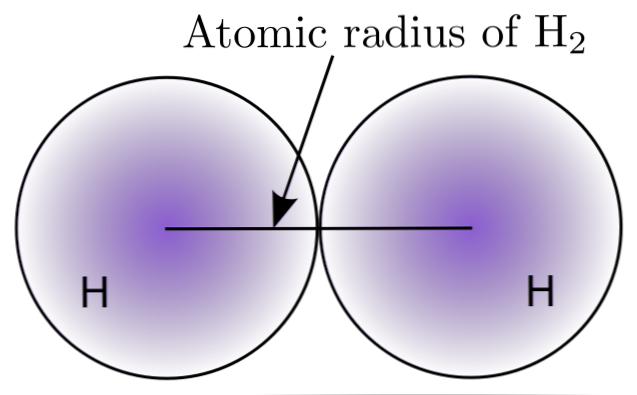
上の画像では、電子が核から離れるにつれて電子が見つかる確率がどのように減少するかがわかります。核間距離を2で割って原子半径を求めます。次に、原子を球形にして、球の体積を計算する式を使用します。
V =(4/3)(Pi)r3
この式で、rはH分子について決定された原子半径です。2. この不正確な方法で計算されたVの値は、たとえばHと見なされた場合に変わる可能性があります。2 液体または金属状態。しかしながら、原子の形状がそれらの相互作用において理想的な球から遠く離れているので、この方法は非常に不正確です。.
固体中の原子体積を決定するために、配置に関する多くの変数が考慮され、そしてそれらはX線回折研究により得られる。.
追加の式
モル質量は、化学元素の原子1モルを含む物質の量を表します。.
その単位はg / molです。一方、密度とは、要素1 gを占有する体積のことです。g / mL。原子体積の単位はmL / molなので、目的の単位に到達するには変数を使用する必要があります。
(g / mol)(mL / g)= mL / mol
または同じことは何ですか:
(モル質量)(1 / D)= V
(モル質量/ D)= V
したがって、元素の原子1モルの体積は簡単に計算できます。球状体積の公式では個々の原子の体積が計算されます。最初からこの値に達するには、Avogadroの数(6.02・10)を介して変換が必要です。-23).
周期表における原子体積の変化?
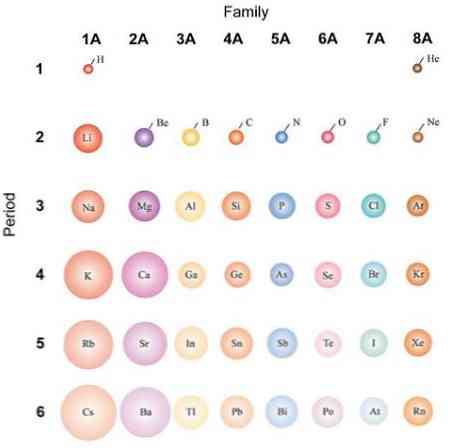
原子が球形と見なされる場合、その変動は原子半径で観察されるものと同じになります。代表的な元素を示す上の画像では、原子が右から左へ矮星であることが示されています。代わりに、上から下に向かって、これらはより大きくなります.
これは、同じ期間に核が右に移動するときに陽子が取り込まれるためです。これらの陽子は外部電子に引力を及ぼし、それが実効的な原子核電荷を感じる。ef, 実際の原子価Zよりも小さい.
内層の電子は外層の電子を反発し、これらに対する核の影響を減少させる。これはスクリーン効果として知られています。同じ期間には、スクリーン効果は陽子の数の増加を打ち消すことができないので、内層の電子は原子の収縮を妨げません。.
しかしながら、グループに降りることによって、新しいエネルギー準位が可能になり、それは電子が原子核からより遠くに周回することを可能にする。また、内層の電子数が増加し、核が再び陽子を追加すると、その遮蔽効果が減少し始めます。.
これらの理由から、8A族(または18族)の小さい原子とは異なり、1A族が最も嵩高い原子を有することが分かる。.
遷移金属の原子量
遷移金属の原子は、電子を内部軌道に取り込む。d。スクリーン効果の増加、そして実際の核電荷Zの増加はほぼ等しく相殺され、その結果それらの原子は同じ期間に同じ大きさを保つ。.
言い換えれば、ある期間において、遷移金属は類似の原子体積を示す。ただし、これらの小さな違いは、金属結晶を定義するときには非常に重要です(あたかもそれらが金属大理石であるかのように)。.
例
元素の原子体積を計算するために2つの数式があり、それぞれに対応する例があります。.
例1
水素の原子半径-37 pm(1ピコメートル= 10)-12年m) - そしてセシウム-265 pm-、その原子体積の計算.
球形体積の公式を使用すると、次のようになります。
VH=(4/3)(3.14)(37 pm)3= 212.07 pm3
VCs=(4/3)(3.14)(265 pm)3= 77912297,67 pm3
しかし、高温計で表現された体積は法外なので、それらはオングストロームの単位に変換され、それらに変換係数(1Å/ 100pm)を掛けます。3:
(212.07午後3)(1Å/ 100pm)3= 2.1207×10-4 Å3
(77912297,67 pm3)(1Å/ 100pm)3= 77,912Å3
したがって、Hの小さな原子とCの嵩高い原子とのサイズの違いは、数値的に明らかなままです。これらの計算は、原子が完全に球形であるという主張の下での近似にすぎず、現実に直面してさまようことに留意しなければならない。.
例2

純金の密度は19.32 g / mL、モル質量は196.97 g / molです。金原子1モルの体積を計算するために式M / Dを適用すると、次のようになります。
VAu=(196.97g / mol)/(19.32g / mL)= 10.19mL / mol
つまり、1モルの金原子が10.19 mLを占有しますが、金原子は具体的にどのくらいの体積を占有しますか。そしてそれを午後の単位で表現する方法3? これには、単に以下の変換係数を適用するだけです。
(10.19 mL / mol)・(mol / 6.02・10)-23 原子)・(1 m / 100 cm)3・(1 pm / 10-12年m)3= 16,92・106 午後3
一方、金の原子半径は166 pmです。前の方法で得られたものと球形体積の公式で計算されたものの両方の体積を比較すると、それらは同じ値を持たないことがわかります。
VAu=(4/3)(3.14)(166 pm)3= 19.15・106 午後3
2つのうちどちらが許容値に最も近いですか?金の結晶構造のX線回折によって得られた実験結果に最も近いもの.
参考文献
- Helmenstine、Anne Marie、Ph.D. (2017年12月9日). アトミックボリュームの定義. 2018年6月6日、以下から取得:thoughtco.com
- メイフェア、アンドリュー。 (2018年3月13日). 原子の体積を計算する方法偵察. 2018年6月6日、sciencing.comから取得。
- ウィキキッズ株式会社(2018). Lothar Meyer原子体積曲線. 2018年6月6日、以下から取得しました:wonderwhizkids.com
- ルーメン周期的傾向原子半径2018年6月6日、コースから取得
- カミロJ.ダーピッチ. 体積と原子密度. es-puraquimica.weebly.comから、2018年6月6日に取得されました
- ホワイト、デイビス、ペック、スタンレー。化学(第8版)。 CENGAGEラーニング、p 222-224.
- CK-12財団。 (2010年2月22日)原子サイズの比較[図データ] 2018年6月6日、commons.wikimedia.orgから取得しました。
- CK-12財団。 (2010年2月22日). Hの原子半径2. [図データ] 2018年6月6日、commons.wikimedia.orgから取得しました。


