ヨウ素酸カリウムの性質、構造、用途およびリスク
の ヨウ素酸カリウム またはヨウ素酸カリウムはヨウ素の無機化合物、具体的には塩であり、その化学式はKIOです。3. ハロゲン(F、Cl、Br、I、As)の群の元素であるヨウ素は、この塩において+5の酸化数を有する。このため、それは強力な酸化剤です。 KIO3 水性媒質中で解離してKイオンを生成する+ とIO3-.
それは水酸化カリウムをヨウ素酸と反応させることによって合成される:HIO3(aq)+ KOH(s)=> KIO3(aq)+ H2O(l)また、ヨウ素分子を水酸化カリウムと反応させることによっても合成することができる。2(s)+ 6KOH(s)=> KIO3(水溶液)+ 5KI(水溶液)+ 3H2O(l).

索引
- 1物理的および化学的性質
- 1.1酸化剤
- 2化学構造
- 3ヨウ素酸カリウムの用途と用途
- 3.1治療的使用
- 3.2業界での使用
- 3.3分析用
- 3.4レーザー技術での使用
- 4ヨウ素酸カリウムの健康リスク
- 5参考文献
物理的および化学的性質
それは微結晶と単斜晶系の結晶構造を有する無臭の白色固体である。それは3.98g / mLの密度、214g / molの分子量を有しそして赤外線(IR)スペクトルに吸収帯を有する。.
融点は833ºK(560ºC)で、Kイオン間の強いイオン相互作用と一致しています。+ とIO3-. 高温では熱分解反応を起こし、分子状酸素とヨウ化カリウムを放出します。
2KIO3(s)=> 2KI(s)+ 3O2(g)
水中では4.74g / 100mLから0℃まで、100℃では最大32.3g / 100mLまで変化する溶解度を持ち、無色の水溶液を生成します。また、アルコールや硝酸には不溶ですが、希硫酸には可溶です.
水との親和性はそれほど高くないため、なぜそれが吸湿性ではなく、水和塩の形で存在しないのかを説明します(KIO)。3・H2O).
酸化剤
その化学式によって示されるように、ヨウ素酸カリウムは3個の酸素原子を有する。これは強く電気陰性の元素であり、そしてこの特性のために、それはヨウ素を取り巻く雲の中の電子的な欠陥を「発見」します。.
この欠乏、または場合によっては寄与は、ヨウ素の酸化数(±1、+ 2、+ 3、+ 5、+ 7)として計算することができ、この塩の場合は+5である。.
これはどういう意味ですか?その電子を生成することができる種の前に、ヨウ素はそれらのイオン型でそれらを受け入れるでしょう(IO3-)ヨウ素分子になり、0に等しい酸化数を持つ.
この説明に従えば、ヨウ素酸カリウムは多くの酸化還元反応において還元剤と強く反応する酸化化合物であると判断することができる。これらすべてのうち、1つはヨウ素時計として知られています.
ヨウ素時計は、遅いステップと速いステップの酸化還元プロセスで構成されています。この場合、速いステップにはKIOソリューションが使用されています。3 デンプンを加えた硫酸中で。次に、デンプン - 一度生成され、その構造種の間に固定されていますI3-- 溶液を無色から濃い青に変える.
IO3 - + 3 HSO3 - →私は - + 3 HSO4 -
IO3 - + 5私 - + 6 H+ →3私2 + 3 H2○
私は2 + HSO3 - + H2O→2私 - + HSO4 - + 2 H+ (でんぷん効果による濃紺)
化学構造
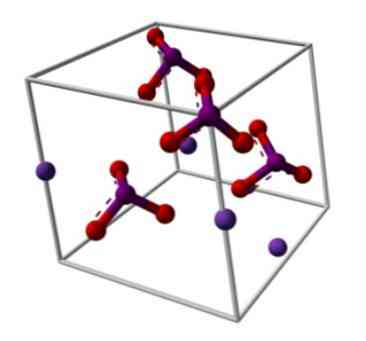
ヨウ素酸カリウムの化学構造は上の画像に示されています。 IOアニオン3- Kイオンは赤と紫の球の「三脚」で表されます。+ それらは紫色の球で表されます.
しかし、これらの三脚はどういう意味ですか?これらのアニオンの正しい幾何学的形状は、実際には三角錐であり、そこでは酸素が三角底を形成し、ヨウ素内の共有されていない電子対が上方を指し、空間を占有しIOリンクを強制的に下げます。リンクI = O.
この分子構造はspハイブリダイゼーションに対応する。3 中心ヨウ素原子の。しかしながら、別の見方は、酸素原子の一つがヨウ素の "d"軌道と結合を形成し、実際にはsp混成体であることを示唆している。3日2 (ヨウ素はその原子価殻を拡張する "d"軌道を持つことができます).
この塩の結晶は、それらを支配する異なる物理的条件の結果として、構造相(単斜晶以外の他の配置)の転移を受ける可能性がある。.
ヨウ素酸カリウムの用途と用途
治療的使用
ヨウ素酸カリウムは通常甲状腺の放射能の蓄積を防ぐために使われます。 131私は、この同位体が甲状腺の機能の構成要素として甲状腺によるヨウ素摂取量の決定に使われるとき.
同様に、ヨウ素酸カリウムは粘膜感染症の局所消毒薬(0.5%)として使用されています.
業界での使用
それはヨウ素サプリメントとして家畜の飼料に添加されています。したがって、業界ではヨウ素酸カリウムが小麦粉の品質を向上させるために使用されています.
分析用
分析化学では、その安定性のおかげで、チオ硫酸ナトリウム標準溶液の標準化における主要な標準として使用されています(Na2S2○3)試料中のヨウ素濃度を測定するため.
これは、ヨウ素の量が容量法(滴定)によって知ることができることを意味します。この反応において、ヨウ素酸カリウムはヨウ化物イオンを急速に酸化する。-, 次の化学式によって
IO3- + 5I- + 6時間+ => 3I2 + 3H2○
ヨウ素、私は2, はNaの解と題される2S2○3 その標準化のために.
レーザー技術での使用
興味深い圧電、焦電気、電気光学、強誘電特性、およびKIO結晶の非線形光学における研究が実証され、裏付けられています。3. これは、電子分野およびこの化合物を用いて製造された材料のためのレーザー技術において大きな可能性をもたらす。.
ヨウ素酸カリウムの健康リスク
高用量では、口腔粘膜、皮膚、目、気道に刺激を引き起こす可能性があります。.
動物におけるヨウ素酸カリウムの毒性の実験は、経口で供給された、0.2〜0.25 g / kg体重の用量で絶食している犬において、化合物が嘔吐を引き起こすことを観察することを可能にしました.
これらの嘔吐が回避されると、それは動物の状況を悪化させる原因となります。それは、死亡前に食欲不振と衰弱を引き起こすからです。彼の剖検は肝臓、腎臓および腸粘膜の壊死性病変を観察することを可能にした.
酸化力があるため、可燃性物質と接触すると火災の危険性があります。.
参考文献
- デイ、R.、アンダーウッド、A. 定量分析化学 (第5版)。ピアソンプレンティスホール、p-364.
- Muth、D.(2008)。レーザー。取得元:flickr.com
- ケミカルブック(2017). ヨウ素酸カリウム. 2018年3月25日、化学ブックから検索:chemicalbook.com
- PubChem。 (2018)。ヨウ素酸カリウム2018年3月25日にPubChemから取得:pubchem.ncbi.nlm.nih.gov
- メルク(2018)。ヨウ素酸カリウム2018年3月25日、メルクより
- merckmillipore.com
- ウィキペディア(2017)ヨウ素酸カリウム2018年3月25日、ウィキペディアから取得:en.wikipedia.org
- M M Abdel Kader他。 (2013)。 KIOにおける電荷輸送機構と低温相転移3. J. Phys。:Conf。Ser。423 012036


