酢酸ナトリウムの処方、製法、特性、リスクおよび用途
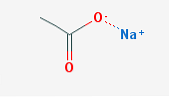
の 酢酸ナトリウム, エタン酸ナトリウム(NaOAcと略される)としても知られる、酢酸のナトリウム塩である。その化学式はCHです3ナトリウムイオンと酢酸イオンの間にイオン結合を持つCOONa.
この化合物は植物や動物の組織に自然に存在します。それは、無水または三水和物のいずれの形態でも見出すことができる。 Na +とCHの両方のイオン3COO- 体内に存在し、重要な機能を果たします。体内水分の調整剤としてのナトリウムイオンおよび水素受容体としての酢酸イオン.
索引
- 1準備
- 2物理的および化学的性質
- 3反応性と危険性
- 4取扱い及び保管
- 5用途と用途
- 6参考文献
準備
酢酸ナトリウムは、誰にとっても簡単で利用しやすい方法で調製できる化合物です。結晶化は固体状態の水に似ているため、一般的にその調製は「ホットアイス実験」として知られています(科学者、2016)。.
酢酸ナトリウムを準備するには、酢(酢酸)と炭酸ナトリウムまたは重炭酸ナトリウムだけが必要です。それは反応に応じて二酸化炭素を放出するので、単純に酢に重炭酸塩を追加し、発泡反応を生成します.
CH3COOH + NaHCO3 →CH 3 COONa + H2CO3
H2CO3 →CO2 + H2○
炭酸塩または重炭酸ナトリウムは、次の反応に従って酢酸ナトリウムおよび水が生成される水酸化ナトリウム(アルカリ)で置き換えることができる。
CH3COOH + NaOH→CH 3 COONa + H2○
この反応は発泡を引き起こさないが、水酸化ナトリウムは重炭酸塩よりも取り扱いが難しいという欠点を有する。.
結晶化の効果(または熱い氷の効果)を得るために、溶液は、重炭酸塩を過剰に溶解するためにそれを加熱することによって過飽和にされなければならない。次いで蓋をした容器を冷却し、次いで再結晶する。続いて、結晶を濾過し、そして貯蔵のために粉砕する(degroof、S.F.)。.
物理的および化学的性質
酢酸ナトリウムは酢臭のある白い吸湿性ガラスです。.

無水形態の化合物の場合、それは82.03g / molの分子量を有しそして密度は1.5g / mlである。その融点は324℃であり、その沸点は881.4℃です.
その三水和形態では、それは136.03g / molの分子量および1.45g / mlの密度を有する。融点はそれぞれ58℃と122℃に劇的に低下します.
酢酸ナトリウムは非常に水に溶けやすいです。三水和物形態の溶解度は、摂氏20度で100mlの水中に46.5gの酢酸ナトリウムであり、その無水形態では、100mlの水当たり123グラムを溶解することができる(National Center for Biotechnology Information、2017)。 ).
両形態はアセトン、メタノール、ヒドラジンに可溶であり、そして三水和物形態はエタノールに可溶である。酢酸ナトリウムは単斜晶系結晶構造を有する(Royal Society of Chemistry、2015).
酢酸ナトリウムは酢酸の共役塩基ですので、pHを制御するために、緩衝液を調製するために酢酸/酢酸ナトリウムの溶液を使用することができます.
水中の酢酸ナトリウム溶液は弱アルカリ性です。熱が摂氏324度を超えると、この塩は分解して酢酸ヒュームを生成します。.
反応性と危険性
酢酸ナトリウムは安定な化合物として分類され、酸化剤とは相容れない。加熱すると酢酸の蒸気が発生し、COが放出される2. この化合物は高温で可燃性であり、COとCOを放出する。2.
酢酸ナトリウムの安全性はラットやマウスの動物モデルで広く研究されています。経口投与した場合、ラットの母集団の半分を殺す致死量はラット体重1kgあたり3530mgの酢酸ナトリウムである。.
摂取せずに吸入した場合、ラットの人口の半分を殺すのに必要な量はもっと多く、1時間あたり30 g / m 3以上.
マウスでは、ラットの酢酸ナトリウムの摂取と同様に、3200 mg / kg体重の皮下または皮下注射によってマウスの母集団の半分が死亡します。.
しかしながら、マウスに経口投与した場合、それらはラットよりはるかに耐えることができます。 6891 mg / kg体重のマウスの母集団の半分の致死量.
ヒトでは、酢酸ナトリウムの吸入は咳やのどの痛みを引き起こす可能性がありますが、皮膚や目に直接触れると発赤や刺激を引き起こす可能性があります。しかしながら、そして一般的に、ヒトにおける毒性は最小限である(WASSERMAN、2015).
腹痛、吐き気、嘔吐を伴う消化管の刺激を引き起こし、泌尿器系に影響を与える可能性があります。化合物を吸入すると気道を刺激することがあります。症状としては、咳、のどの痛み、息切れ、胸痛などがあります。.
目に入った場合は、コンタクトレンズを点検し、取り除いてください。目は直ちに少なくとも15分間多量の水で洗う必要があります。冷たい水を使うことができます。刺激が生じた場合は医師の診察を受けるべきである.
皮膚に触れた場合は、石鹸と水で洗ってください。冷たい水を使うことができます。刺激された皮膚は皮膚軟化剤で覆われています。アイコンタクトと同様に、刺激が生じた場合は医師の診察を受けるべき.
吸入した場合は、被害者を涼しい場所に移動する必要があります。呼吸していない場合は、人工呼吸を行うべきです。呼吸が困難な場合は、酸素を供給しなければなりません。もう一度、すぐに医師の診察を受ける必要があります.
摂取した場合、医療従事者の明示的な指示がない限り、嘔吐は誘発されるべきではありません。意識のない人には決して口から何も与えないでください。.
シャツの襟、ネクタイ、ベルトなどのゆったりとした服はゆるめてください。症状が現れた場合は医師の診断を受けるべきである(化学物質等安全データシート無水酢酸ナトリウム、2013).
取り扱いと保管
-化合物は熱や発火源から遠ざける必要があります。
-空の容器は火災の危険をもたらし、換気フードの下で残留物を蒸発させる
-電気機器は火花を避けるために接地しなければなりません
-ほこりを飲み込まないでください。
-適切な防護服を着用してください
-換気が不十分な場合は、適切な呼吸装置を着用する必要があります。
-摂取した場合は、直ちに医師のところに行き、容器またはラベルを見せるべきです。
-試薬は、酸化剤や酸などの不適合な物質から遠ざけてください。.
-容器を涼しく換気のよい場所に保管することに加えて、容器を密閉しておく.
用途とアプリケーション
酢酸ナトリウムは非常に多様な産業で使用されています。繊維工業では、酢酸ナトリウムはアニリン染料を使用しながら、硫酸の廃棄物流を中和しそしてフォトレジストとしても中和する。これは完成した生地の品質を向上させます.
写真では、酢酸ナトリウムは現像液の一部であり、フォトレジストとして機能します。酢酸ナトリウムは、環境にやさしく、水浸透に対してコンクリートをシールするために一般的に使用されているエポキシ代替品よりも安価でありながら、シーラントとして作用することによってコンクリートへの水による損傷を軽減するために使用される。.
クロムなめしの酸洗い剤でもあり、合成ゴムの製造におけるクロロプレンの加硫を防ぐのに役立ちます。使い捨て綿パッドの綿加工では、静電気の蓄積を防ぐために酢酸ナトリウムが使用されています.
食品に添加された酢酸ナトリウムは、保存料、および香料として機能します。特に、酢酸ナトリウム入りポテトチップスは独特の「塩と酢」の風味を持っています.
酢酸ナトリウムは、保温パッド、ハンドウォーマー、ホットアイスにも使用されています。三水和物の酢酸ナトリウム結晶は58.4℃で融解し、それらの結晶水に溶解する。.
融点を超えて加熱され、続いて冷却されると、水溶液は過飽和になる。この溶液は結晶を形成することなく室温まで冷却することができます。.
金属ディスクを加熱パッドに押し込むことにより、核形成中心が形成され、溶液を結晶化させて固体酢酸ナトリウム三水和物に戻す。結晶化の結合形成過程は発熱的である。融解潜熱は約264-289 kJ / kgです。.
不可逆的な化学反応に依存するものなど、一部のタイプのヒートパックとは異なり、酢酸ナトリウムのヒートパケットは、結晶が完全に溶解して結晶が完全に溶解するまでパックを沸騰水に数分間浸すことで簡単に再利用できますパックが室温に達するまでゆっくり冷却すること.
酢酸ナトリウムおよび酢酸の溶液は、比較的一定のpH、生化学的研究反応ならびに石油産業および化粧品産業の両方にとって有用な性質を維持するための緩衝剤として作用する。.
酢酸ナトリウムは、小さな核酸の沈殿に使用できます。この沈殿は、flashPAGEの分画後に低機能の緩衝液などの希釈溶液から小さな核酸を濃縮するために使用できます。.
2μg未満の核酸がflashPAGEシュレッダーにロードされるとき、ランニングバッファーからの核酸の最大の回収のために、酢酸ナトリウム/エタノールによる沈殿が一晩アクリル酸アミドまたはグリコーゲンのような媒体で推奨されます。遅い.
担体としてのグリコーゲンの使用は、DNAチップの分析に使用されるであろう試料には推奨されない(小核酸の酢酸ナトリウム沈殿、S.F.)。.
医学の分野では、酢酸ナトリウム溶液は、高血中濃度および/または低ナトリウム濃度の患者を治療します.
ナトリウムは細胞外液の主な陽イオンです。それは約140mEq /リットルのその通常の血漿濃度で総カチオンの90%以上を構成する。ナトリウムイオンは、体内水分量とその分布の制御に重要な役割を果たしています(Sodium Acetate、2010)。.
酢酸塩は水素イオン受容体です。それはまた、肝臓における代謝変換のための重炭酸塩(HCO 3 - )の代替供給源としても役立つ。重度の肝疾患がある場合でも、この変換は容易に進行することが示されています.
水中に希釈した酢酸ナトリウムの注射剤を電解質補充剤として静脈内に投与する。各20mlは、40mEqのナトリウム(Na +)およびアセテート(HCO)を提供する3.28gの酢酸ナトリウムを含む。3-)溶液は静菌剤、抗微生物剤または添加緩衝液を含まない。 pH調整のために酢酸を含んでいてもよい(pHは6.5(6.0〜7.0))。浸透圧濃度は4 mOsmol / ml(計算値)です。.
この溶液は、静脈内使用のための大量輸液への添加のためのナトリウムイオン(Na +)を提供するための塩化ナトリウムの代替として考えられている(Sodium Acetate、2009)。.
ナトリウムイオンを含む溶液は、特にうっ血性心不全、重度の腎不全、およびナトリウム貯留を伴う浮腫がある臨床状態の患者の場合には、細心の注意を払って使用する必要があります。.
腎機能障害のある患者では、ナトリウムイオンを含む溶液を投与するとナトリウム貯留が生じることがあります。酢酸イオンを含む溶液は、代謝性または呼吸性アルカローシス患者には細心の注意を払って使用する必要があります.
重度の肝不全など、このイオンのレベルの増加または使用の障害がある状態では、アセテートを細心の注意を払って投与する必要があります。.
参考文献
- (S.F.)。家庭用食材から酢酸ナトリウムを作る方法レクペラードデインストラクタブル:instructables.com.
- 製品安全データシート酢酸ナトリウム無水。 (2013年5月21日)。 sciencelabから取得しました:sciencelab.com.
- 国立バイオテクノロジー情報センター(2017年3月4日)。 PubChem化合物データベース。 CID = 517045。 PubChemから取得.
- 化学の王立協会。 (2015)酢酸ナトリウムchemspider.comから取得.
- 科学者、D。 (2016年8月12日)。 "HOT ICE" - 素晴らしい実験youtube.comから取得しました.
- 酢酸ナトリウム(2009年5月19日)。 rxlistから取得.
- 酢酸ナトリウム(2010年4月) drugs.comから回収.
- 酢酸ナトリウム(2005-2017)。 softschools.comから回復しました.
- 小核酸の酢酸ナトリウム沈殿(S.F.)。サーモフィッシャーから回収.
- WASSERMAN、R.(2015年8月16日)。酢酸ナトリウム塩とは何ですか? livestrongから取得しました:livestrong.com.


