硫化水素(H2S)の特性、リスクと用途
の 硫化水素 硫化水素(H2S)それは溶液中のヒドラジド酸(H2S(aq)).
この化合物の水中での溶解度が低いにもかかわらず、スルフヒドリル酸についての考慮がなされている。その構造は図1に示されている(EMBL-EBI、2005)。.
したがって、硫化水素は水にわずかに溶けます。溶解すると酸硫化物イオンまたは水硫化物(HS)を形成します。-)硫化水素、または硫化水素の水溶液は無色で、空気に触れると水に溶けない元素状の硫黄をゆっくり酸化します。.
硫黄ジアニオンS2- それは強アルカリ性水溶液中にのみ存在する。それはpKa> 14を持つ非常に基本的なものです.
H2Sは、特に高温で、元素状硫黄が有機材料と実質的に接触するところから生じる。硫化水素は、水と化学的に関連する共有結合水素化物です。2O)、酸素と硫黄は周期律表と同じ族で生成されるので.
湿地や下水道の中など、酸素がない状態でバクテリアが有機物を分解すると(嫌気性消化プロセスと共に)しばしば起こります。それはまた火山ガス、天然ガスおよびいくつかの井戸水で発生します.
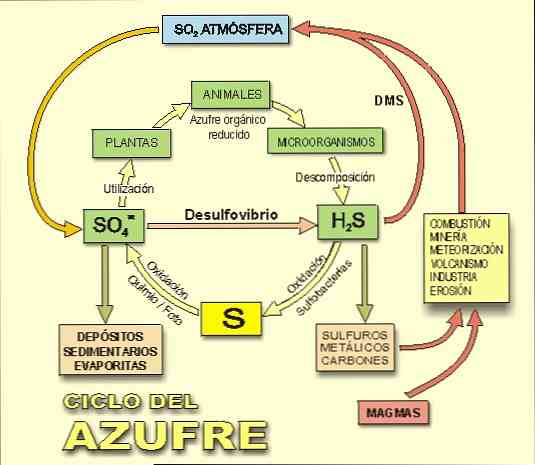
硫化水素は、硫黄循環、つまり地球上の硫黄の生物地球化学的循環の中心的な要素であることを心に留めておくことも重要です(図2)。.
上記のように、硫黄低減および硫酸還元細菌は、硫黄または硫酸を硫化水素に還元することによって、酸素の不在下で水素または有機分子から酸化エネルギーを得る。.
他の細菌は硫黄を含むアミノ酸から硫化水素を放出する。酸化剤として酸素または硝酸塩を使用して、硫化水素を燃料として使用し、それを元素状の硫黄または硫酸塩に酸化することができます。.
純粋な硫黄バクテリアと緑の硫黄バクテリアは、光合成の電子供与体として硫化水素を使用して、元素硫黄を生成します。.
事実、このモードの光合成は、水を電子供与体として使用して酸素を放出するシアノバクテリア、藻類、植物のモードよりも古くなっています(Human Metabolome Database、2017)。.
索引
- 1硫化水素が発生する場所?
- 2物理的および化学的性質
- 3反応性と危険性
- 3.1吸入
- 3.2皮膚接触
- 3.3アイコンタクト
- 4つの用途
- 4.1 1-硫黄の生産
- 4.2 2-分析化学
- 4.3 3-その他の用途
硫化水素が発生する場所?
硫化水素(H2S)は、原油、天然ガス、火山ガス、温泉などに自然に発生します。それはまた有機物のバクテリアによる分解からも起こり得る。それはまた人間および動物の無駄によって作り出されます.
口や胃腸管に見られるバクテリアはバクテリアから硫化水素を生成し、植物や動物のたんぱく質を含む物質を分解します。.
硫化水素は、食品加工、コークス炉、クラフト製紙工場、製革所、石油精製所などの産業活動からも発生する可能性があります(2011年毒性物質・疾病登録局)。.
物理的および化学的性質
硫化水素は腐った卵の臭いが強い無色のガスです。硫化水素の水溶液は、特徴的な香りのない無色です。.
化合物は34.1g / molの分子量を有し、水溶液は1.343g / mlの密度を有する。それは-82℃の融点および-60℃の沸点を有する。これは水にわずかに溶け、20℃で1リットルあたりわずか4グラムのこの溶媒を溶解することができる(Royal Society of Chemistry、2015).
硫化水素は酸としてそして還元剤として反応する。それは、二フッ化酸素、五フッ化臭素、三フッ化塩素、二塩化酸化物およびフマル酸銀と接触して爆発する。酸素の存在下で銅粉にさらされると、引火して爆発する可能性がある.
それは他の粉末金属と同様に反応することができます。金属酸化物および過酸化物(過酸化バリウム、三酸化クロム、酸化銅、二酸化鉛、二酸化マンガン、酸化ニッケル、酸化銀、二酸化銀、三酸化タリウム、過酸化ナトリウム、酸化水銀、酸化カルシウム).
それは臭素酸銀、次亜塩素酸鉛(II)、クロム酸銅、硝酸、酸化鉛(IV)および酸化物で点火されます。錆びた鉄パイプを通過すると発火する可能性があります。塩基と発熱反応する.
ソーダ石灰、水酸化ナトリウム、水酸化カリウム、水酸化バリウムとの反応熱は、空気/酸素の存在下で未反応部分の発火または爆発を引き起こす可能性がある(HYDROGEN SULFIDE、2016).
反応性と危険性
H2Sは引火性が高く、非常に有毒ですが、安定した化合物と見なされます。.
この化合物は空気より重く、発火源までかなりの距離を移動して後退することができます。広範囲の空気と爆発性混合物を形成することができる.
五フッ化臭素、三フッ化塩素、三ヨウ化窒素、三塩化窒素、二フッ化酸素、塩化フェニルジアゾニウムとも爆発的に反応する。.
分解するまで加熱すると、非常に有毒なフューム(硫黄酸化物)を放出する。強酸化剤、金属、強硝酸、五フッ化臭素、三フッ化塩素、三ヨウ化窒素、三塩化窒素、二フッ化酸素、および塩化フェニルジアゾニウムを含む多くの材料との互換性がありません。.
硫化水素(H2S)は、特に石油産業における職業上の毒性暴露の多くの事件の原因である。 Hの臨床効果2Sはその濃度と暴露期間に依存します.
H2Sが500〜1000ppmを超えるとすぐに致命的になりますが、10〜500ppmのような低濃度にさらされると、鼻炎から急性呼吸不全までさまざまな呼吸器症状を引き起こす可能性があります。.
H2Sは複数の臓器にも影響を及ぼし、神経系、心臓血管系、腎臓、肝臓、血液系に一時的または恒久的な障害を引き起こす可能性があります。.
Hへの職業的曝露の事例が提示されている2それはいくつかの臓器の関与、急性呼吸不全、肺炎の組織化および急性敗血症と同様のショックをもたらす。この場合、患者はまた、軽度の閉塞性および制限性の肺疾患および末梢神経障害を発症した(Al-Tawfiq、2010年)。.
吸入
吸入した場合は、屋外に持ち帰り、呼吸しやすいように安静にしてください。呼吸していない場合は、人工呼吸を行ってください。呼吸が困難な場合は、訓練を受けた担当者が酸素を供給するようにしてください。.
肌に触れる
皮膚に触れた場合は、大量の水で洗ってください。加圧液体は凍傷を引き起こす可能性があります。加圧液体にさらす場合は、凍結ゾーンを直ちに41℃を超えない温水で加熱する必要があります。.
水温は普通の肌に耐えられるものでなければなりません。皮膚のウォームアップは少なくとも15分間、または通常の着色と感覚が患部に戻るまで維持する必要があります。大量のばく露の場合は、暖かい水でシャワーを浴びながら服を脱ぐ.
アイコンタクト
目に入った場合は、少なくとも15分間水で十分に洗い流してください。まぶたを開いて、眼球から離して、すべての表面を徹底的にすすいでください。.
経口摂取は可能性のある暴露経路とは見なされません。他のすべての症例では、直ちに医師の診察を受ける必要があります(Praxair、2016)。.
用途
1-硫黄の生産
クラウスの硫黄回収装置は、燃焼炉、廃熱ボイラー、硫黄凝縮器、一連の触媒段から構成され、それぞれが再加熱、触媒床および硫黄凝縮器を採用しています。典型的には、2つまたは3つの触媒段階が用いられる。.
クラウス法は二段階反応を通して硫化水素を元素状硫黄に変換する.
第一段階は、硫化水素の約三分の一を二酸化硫黄に変換するための供給ガスの制御された燃焼および二酸化硫黄で燃焼されていない硫化水素の非触媒反応を含む。.
第二段階では、クラウス反応、硫化水素と二酸化硫黄が触媒上で反応して硫黄と水を生成します。.
燃焼空気の量は硫黄回収率を最大にするために、すなわち下流の反応器を通して2:1硫化水素対二酸化硫黄の適切な反応化学量論を維持するために厳密に制御される。.
典型的には、最大97%の硫黄回収率を達成することができる(米国国立医学図書館、2011年)。.
2-分析化学
一世紀以上の間、硫化水素は分析化学において、金属イオンの定性的無機分析において重要であった。.
これらの分析では、H 2 Sにさらした後の溶液から重金属(および非金属)イオン(たとえば、Pb(II)、Cu(II)、Hg(II)、As(III))が沈殿します。得られた沈殿物は幾らかの選択性をもって再び溶解し、従って同定される。.
3-その他の用途
この化合物は、Girdler硫化物プロセスによって、重水と普通の水を分離するためにも使用されます。.
エクセター大学の科学者たちは、少量の硫化水素ガスに細胞が曝されるとミトコンドリアの損傷を防ぐことができることを発見しました.
細胞がこの疾患でストレスを受けると、酵素が細胞に引き寄せられて少量の硫化水素が生成されます。この研究は、脳卒中、心臓病、および関節炎の予防により多くの影響を及ぼす可能性があります(Stampler、2014)。.
硫化水素は、赤ワインに含まれる抗酸化物質であるレスベラトロールに似た性質を持つ、細胞内の破壊的な化学物質をブロックすることで抗老化作用を持つ.
参考文献
- 毒性物質および疾病登録機関。 (2011年3月3日). 硫化水素硫化カルボニル. atsdr.cdc.govから取得.
- Al-Tawfiq、B. D.(2010)。成人男性における硫化水素曝露. サウジアラビアの年鑑30(1) , 76〜80.
- EMBL-EBI (2005年12月13日). 硫化水素. ebi.ac.ukから回復.
- 百科事典ブリタニカ。 (S.F.). 硫化水素. britannica.comから回収.
- ヒトメタボロームデータベース(2017年3月2日). 硫化水素 . hmdb.caから取得.
- 硫化水素. (2016) cameochemicals.noaa.govから取得.
- (2016年10月17日). 硫化水素安全データシート. praxair.comから回復しました.
- 化学の王立協会。 (2015年). 硫化水素. chemspider.comから取得.
- Stampler、L.(2014年7月11日). 臭い化合物は細胞の損傷を防ぐ可能性がある、研究結果. time.comから取得.
- アメリカ国立医学図書館。 (2011年9月22日). 硫黄、エレメンタル. toxnet.nlm.nih.govから取得.


