リン酸カルシウム(Ca 3(PO 4)2)の構造、性質、形成および用途
の リン酸カルシウム 化学式がCaである無機三級塩3(PO4)2. 式は、この塩の組成がカルシウムとリン酸に対してそれぞれ3:2であると述べている。これは、Caカチオンが示されている下の画像に直接見ることができる。2+ そして陰イオンPO43-. 3 Caごとに2+ POが2つあります43- 彼らと交流する.
一方、リン酸カルシウムは、Ca / P比、ならびに水和度およびpHに応じて変化する一連の塩を指す。事実、存在し合成することができる多くの種類のリン酸カルシウムがある。しかし、命名法に従って文字通り、リン酸カルシウムは三カルシウム、前述の.

Caを含むすべてのリン酸カルシウム3(PO4)2, 彼らはわずかに灰色がかった色調を持つ無地の白です。それらは、粒状、細かい、結晶質であり得、そして約マイクロメートルの粒径を有し得る。そしてさらに、これらのリン酸塩のナノ粒子が調製されており、それを用いて骨のための生体適合性材料が設計されている。.
この生体適合性は、これらの塩が歯の中に、そして要するに哺乳動物の骨組織の中に見出されるという事実によるものである。例えば、ヒドロキシアパタイトは結晶性リン酸カルシウムであり、これは次に同じ塩の非晶質相と相互作用する。.
これは、非晶質および結晶性リン酸カルシウムが存在することを意味します。このため、リン酸カルシウム系の材料を合成する場合、多様性と多様な選択肢は驚くにあたらない。骨の修復に焦点を当てるために、世界中で毎日研究者が関心を持っている材料.
索引
- 1リン酸カルシウムの構造
- 1.1アモルファスリン酸カルシウム
- 1.2家族の残りの部分
- 2物理的および化学的性質
- 2.1名前
- 2.2分子量
- 2.3物理的な説明
- 2.4味
- 2.5融点
- 2.6溶解度
- 2.7密度
- 2.8屈折率
- 2.9訓練の標準エンタルピー
- 2.10保管温度
- 2.11 pH
- 3トレーニング
- 3.1硝酸カルシウムとリン酸水素アンモニウム
- 3.2水酸化カルシウムとリン酸
- 4つの用途
- 4.1骨組織内
- 4.2バイオセラミックセメント
- 4.3医師
- 4.4その他
- 5参考文献
リン酸カルシウムの構造
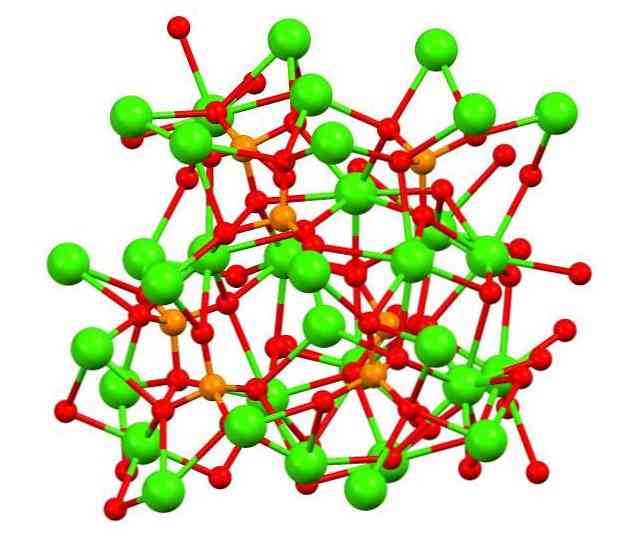
上の図は、不純物としてマグネシウムと鉄を含んでいる可能性がある、奇妙なウィットロック鉱物中の三塩基性カリコリン酸塩の構造を示しています.
一見すると複雑に思えるかもしれませんが、モデルはリン酸塩の酸素原子とカルシウムの金属中心との間の共有相互作用を仮定していることを明確にする必要があります。.
表現としては有効ですが、相互作用は静電気です。つまり陽イオンCa2+ POアニオンに惹かれる43- (Ca2+- O-PO33-)これを念頭に置いて、画像内でカルシウム(緑色の球)が負に帯電した酸素原子(赤色の球)に囲まれている理由は理解されます。.
非常に多くのイオンがあるとき、それは目に見える対称的な配置またはパターンを残しません。 Ca3(PO4)2 低温での採用(T<1000°C) una celda unitaria correspondiente a un sistema cristalino romboédrico; a este polimorfo se le conoce con el nombre de β-Ca3(PO4)2 (β-TCP、英語の頭字語のために).
一方、高温では、多形体α-Caに変換されます。3(PO4)2 その単位格子が単斜晶系に対応する(α-TCP)。さらに高い温度では、多形体α'− Caも形成され得る。3(PO4)2, 六方晶構造のもの.
アモルファスリン酸カルシウム
結晶構造は、リン酸カルシウムについて言及されており、それは塩から予想されることである。しかしながら、それはその定義の厳密な意味で結晶よりも一種の「リン酸カルシウムガラス」に関連した無秩序で非対称な構造を示すことができる。.
これが起こるとき、それはリン酸カルシウムが無定形構造(ACP)を持っていると言われています, アモルファスリン酸カルシウム)何人かの著者は、Caの生物学的特性に責任があるとしてこのタイプの構造を指摘します3(PO4)2 骨組織では、その修復と生体模倣が可能です.
核磁気共鳴(NMR)によるその構造の解明を通して、OHイオンの存在が見出された。- とHPO42- ACPで。これらのイオンは、リン酸塩の1つの加水分解によって形成されます。
PO43- + H2○ <=> HPO42- + OH-
結果として、ACPの真の構造はより複雑になり、そのイオンの組成は次式によって表される。9(PO4)6-x(HPO4)×(OH)×. x = 1の場合、式は次のようになるため、 'x'は水和度を示します。9(PO4)5(HPO4)(OH).
PCAが有し得る異なる構造は、Ca / Pモル比に依存する。すなわち、カルシウムとリン酸塩の相対量であり、それがそれらの結果として生じる組成をすべて変えます。.
家族の残りの部分
リン酸カルシウムは実際には無機化合物のファミリーであり、それは今度は有機マトリックスと相互作用することができる。.
他のリン酸塩は、カルシウムを伴うアニオンを変えることによって「単純に」得られます(PO43-, HPO42-, H2PO4-, OH-)、ならびに固体中の不純物の種類。したがって、それぞれ独自の構造および特性を有する最大11個以上のリン酸カルシウムが、天然または人工的に由来し得る。.
下記はいくつかのリン酸塩とそのそれぞれの構造および化学式です。
-リン酸水素カルシウム二水和物、CaHPO4∙2H2O:単斜晶系.
-リン酸二水素カルシウム一水和物、Ca(H)2PO4)2∙H2O:三斜晶系.
-無水二酸リン酸塩、Ca(H)2PO4)2:三斜系.
-リン酸水素カルシウム(OCP)、Ca8H2(PO4)6:三斜系それはヒドロキシアパタイトの合成における前駆体です.
-ヒドロキシアパタイト、Ca5(PO4)3OH:六角形.
物理的および化学的性質
お名前
-リン酸カルシウム
-リン酸三カルシウム
-二リン酸三カルシウム
分子量
310.74 g / mol.
物理的な説明
無臭の白い固体です.
味
無味.
融点
1670ºK(1391ºC).
溶解度
-水にほとんど溶けない.
-エタノールに不溶.
-希塩酸、硝酸に可溶.
密度
3.14 g / cm3.
屈折率
1,629
トレーニングの標準エンタルピー
4126 kcal / mol.
保管温度
2〜8℃.
pH
50 g / Lのリン酸カルシウムの水性懸濁液中の6-8.
トレーニング
硝酸カルシウムとリン酸水素アンモニウム
リン酸カルシウムを製造または形成するための多数の方法がある。それらのうちの1つは2つの塩、Ca(NO)の混合物から成ります3)2∙4H2O、そして(NH4)2HPO4, 以前はそれぞれ無水アルコールと水に溶解していました。 1つの塩はカルシウムを提供し、他のリン酸塩は.
この混合物からACPが沈殿し、次いでこれをオーブン中800℃で2時間加熱する。この手順の結果として、β- Caが得られる。3(PO4)2. 温度、攪拌および接触時間を注意深く制御することによって、ナノ結晶形成が起こり得る。.
多形体α-Caを形成する3(PO4)2 リン酸塩を1000℃以上に加熱することが必要である。この加熱は他の金属イオンの存在下で行われ、それはこの多形体を室温で使用するのに十分に安定化させる。つまり、安定したメタ状態のままです。.
水酸化カルシウムとリン酸
リン酸カルシウムはまた、水酸化カルシウムとリン酸の溶液を混合することによっても形成することができ、酸塩基中和が起こる。母液を熟成させ、それらを適切に濾過し、洗浄し、乾燥させそしてふるい分けをして半日後に、非晶質リン酸塩の粒状粉末が得られる。.
このACPは高温の生成物を反応させ、以下の化学式に従って変換する:
2Ca9(HPO4)(PO4)5(OH)=> 2Ca9(P2○7)0.5(PO4)5(OH)+ H2O(T = 446.60°C)
2Ca9(P2○7)0.5(PO4)5(OH)=> 3Ca3(PO4)2 + 0.5H2O(T = 748.56°C)
このようにして、β- Caが得られる。3(PO4)2, その最も一般的で安定した多形体.
用途
骨組織内
Ca3(PO4)2 それは骨灰の主要な無機成分です。それは骨置換移植の構成要素であり、これは骨中に存在するミネラルと化学的に類似していることによって説明される.
リン酸カルシウム生体材料は、骨の欠陥を矯正するためにそしてチタン金属プロテーゼのコーティングにおいて使用される。リン酸カルシウムがそれらの上に堆積し、それらを環境から隔離し、チタン腐食プロセスを減速させる.
カルシウムを含むリン酸カルシウム3(PO4)2, それらはセラミック材料の製造に使用されます。これらの材料は生体適合性であり、そして歯周病、歯内感染症および他の状態から生じる歯槽骨の減少を回復するために現在使用されている。.
しかし、それらは慢性細菌感染症がない地域で根尖周囲骨修復を促進するためにのみ使用されるべきです.
自家骨移植片を使用することが不可能である場合、リン酸カルシウムを骨欠損の修復に使用することができる。それを単独で又はポリグリコール酸のような生分解性及び吸収性ポリマーと組み合わせて使用することが可能である。.
バイオセラミックセメント
リン酸カルシウム系セメント(CPC)は骨組織の修復に使用される他のバイオセラミックである。それは、異なる種類のリン酸カルシウムの粉末を水と混合してペーストを形成することによって作られる。ペーストを注入するか、骨の欠陥や窩洞に合わせて調整することができます。.
セメントは成形され、徐々に吸収され、新しく形成された骨に置き換えられます.
医者
-Ca3(PO4)2 それは塩基性塩です、従ってそれは余分な胃酸を中和し、pHを上げるために制酸剤として使用されます。練り歯磨きにおいて、それは歯の再石灰化および骨止血のプロセスを促進するためのカルシウムおよびリン酸塩の供給源を提供する.
-カルシウムを置き換える最も安価な方法はその炭酸塩とクエン酸塩を使うことですが、それは栄養補助食品としても使われます。.
-リン酸カルシウムは、破傷風、潜在性低カルシウム血症および維持療法の治療に使用することができます。また、妊娠中や授乳中のカルシウム補給にも役立ちます.
-放射性同位元素ラジオ(Ra-226)とストロンチウム(Sr-90)による汚染の治療に使用されます。リン酸カルシウムは消化管での放射性同位元素の吸収を阻止し、それによってそれらによって引き起こされる損傷を制限します.
その他
-リン酸カルシウムは鳥の飼料として使われています。さらに、それは歯石を制御するために練り歯磨きに使用されます.
-それは、例えば食卓塩が圧縮されるのを防止するために固結防止剤として使用されます。.
-小麦粉の漂白剤として働きます。その間、ブタのラードでは望ましくない着色を防ぎ、フライパンの状態を改善します.
参考文献
- 桐さん(1998)リン酸カルシウム:構造、組成、溶解度および安定性。で:生物学的および産業システムにおけるAmjad Z.(eds)リン酸カルシウム。 Springer、Boston、MA.
- Langlang Liu、Yanzeng Wu、Chao Xu、Suchun Yu、Xiaopei Wu、およびHonglian Dai。 (2018)。 「ナノβリン酸三カルシウムの合成、キャラクタリゼーションおよび肝細胞癌細胞に対する阻害」、Journal of Nanomaterials、vol。 2018、記事ID 7083416、7ページ、2018年.
- キリストとレイ、クリスチャンの櫛。 (2010)。非晶質りん酸カルシウム生体材料における合成、性質および用途アクタバイオマテリアル、vol。 6(9°)。 pp。 3362-3378 ISSN 1742-7061
- ウィキペディア(2019)。りん酸三カルシウム取得元:en.wikipedia.org
- Abidaら。 (2017)りん酸三カルシウム粉末調製、キャラクタリゼーションおよび圧縮能力地中海ジャーナル・オブ・ケミストリー2017、6(3)、71-76.
- PubChem。 (2019)。リン酸カルシウム。取得元:pubchem.ncbi.nlm.nih.gov
- エルゼビア(2019)。リン酸カルシウム。サイエンスダイレクト。取得元:sciencedirect.com


