リン酸マグネシウム(Mg 3(PO 4)2)の構造、性質および用途
の リン酸マグネシウム は、マグネシウム、アルカリ土類金属およびリン酸オキソアニオンによって形成される無機化合物のファミリーを指すのに使用される用語である。最も単純なリン酸マグネシウムは、Mgの化学式を有する。3(PO4)2. 式は、2つのPOアニオンごとに43- 3つのMgカチオンがあります2+ これらと相互作用する.
また、これらの化合物はオルトリン酸(H)から誘導されたマグネシウム塩として記載することができる。3PO4)言い換えれば、マグネシウムは、それらの無機的または有機的な存在(MgO、Mg(NO)に関係なく、リン酸アニオン間を「被覆」する。3)2, MgCl2, Mg(OH)2, など).

これらの理由から、リン酸マグネシウムはいくつかのミネラルとして発見されることがあります。これらのいくつかは以下のとおりです。catheita -Mg3(PO4)2 ・22H2O-、ストラバイト - (NH4)MgPO4・6H2または、その微結晶が上の画像に表示されています - ホルタライト-Mg2(PO4)(OH) - およびボビエリタ−Mg3(PO4)2・8H2○-.
ボビエリタの場合、その結晶構造は単斜晶系であり、扇形の形状をした結晶性凝集体と大きなロゼットを有する。しかしながら、リン酸マグネシウムは、豊富な構造化学を示すことを特徴としており、これはそれらのイオンが多くの結晶配列をとることを意味する。.
索引
- 1リン酸マグネシウムの形とその電荷の中性
- 1.1他の陽イオンを含むリン酸マグネシウム
- 2つの構造
- 3プロパティ
- 4つの用途
- 5参考文献
リン酸マグネシウムの形態とその電荷の中性
リン酸マグネシウムはHプロトンの置換に由来する3PO4. オルトリン酸がプロトンを失うと、リン酸二水素イオンHとして残る。2PO4-.
マグネシウム塩を生成するために負電荷を中和する方法は?はいMg2+ 2つの正電荷を説明し、次に2つのHが必要です2PO4-. このようにして、二酸リン酸マグネシウム、Mg(H)が得られる。2PO4)2.
その後、酸が2つのプロトンを失うと、リン酸水素イオンが残ります。42-. では、これら2つの負電荷を中和する方法は? Mgのように2+ それは中和するのに2つの負電荷を必要とするだけであり、単一のHPOイオンと相互作用する。42-. このようにして、酸性リン酸マグネシウムが得られる:MgHPO4.
最後に、すべてのプロトンが失われると、リン酸アニオンPOが残ります。43-. これは3つのMgカチオンを必要とする。2+ 結晶性固体に組み立てるためのもう一つのリン酸塩。数式2(-3)+ 3(+ 2)= 0は、マグネシウムとリン酸の化学量論比を理解するのに役立ちます。.
これらの相互作用の結果として、三塩基性リン酸マグネシウムが生成される。3(PO4)2. なぜそれは三基礎的ですか?それはHの3当量を受け入れることができるので+ 再びHを形成する3PO4:
PO43-(AC)+ 3H+(ac) <=> H3PO4(ac)
他のカチオンとリン酸マグネシウム
負電荷の補償はまた他の正の種の参加によって達成することができます.
たとえば、POを無効にする43-, イオンK+, な+, Rb+, NH4+, なども介在して化合物(X)MgPOを形成する。4. XがNHと等しい場合4+, 無水ストルバイト鉱物が形成され、(NH4)MgPO4.
別のリン酸塩が介在して負電荷が増加する状況を考えると、それらを中和するために他の追加のカチオンを相互作用に加えることができる。これにより、多数のリン酸マグネシウム結晶を合成することができます。3RbMg7(PO4)6, 例えば).
構造

上の画像はMgイオン間の相互作用を示しています2+ とPO43- それは結晶構造を定義します。しかしながら、それはむしろリン酸塩の四面体幾何学を実証する像にすぎない。それから、結晶構造はリン酸塩およびマグネシウムの球の四面体を含みます.
Mgの場合3(PO4)2 無水のイオンは、菱面体晶構造を取ります。2+ 6個のO原子で配位している.
上の図は下の画像に示されていますが、青い球体はコバルトであるという表記で、緑色のマグネシウム球体に変更するだけで十分です。
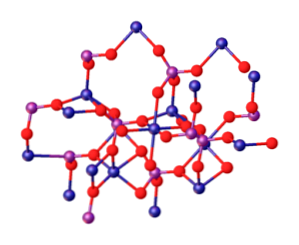
構造の真ん中には、青みがかった球の周りにある6つの赤い球によって形成された八面体があります。.
また、これらの結晶構造は水分子を受け入れることができ、リン酸マグネシウム水和物を形成します。.
これは、それらがリン酸イオン(HOH-O-PO)と水素結合を形成するからである。33-)さらに、各リン酸イオンは最大4つの水素結合を受け入れることができます。つまり、4つの水分子.
Mgのように3(PO4)2 2つのリン酸塩があり、8つの水分子を受け入れることができます(ミネラルbobierritaで起こること)。その結果、これらの水分子は他の分子と水素結合を形成したり、正のMg中心と相互作用したりする2+.
プロパティ
それは結晶性の菱形のプレートを形成している、白い固体です。また、無臭、無味.
それは、その大きな結晶格子エネルギーのために、たとえそれが熱いときでも、水に非常に不溶である。これは、多価Mgイオン間の強い静電相互作用の産物です。2+ とPO43-.
すなわち、イオンが多価であり、それらのイオン半径があまり大きく変化しない場合、固体はその溶解に対する耐性を示す。.
それは1184℃で融解し、これも強い静電相互作用の指標である。これらの特性は、それがどれだけの水の分子を吸収するか、そしてホスフェートがそのプロトン化形態のいくつかで見出されるかどうか(HPO42- またはH2PO4-).
用途
それは便秘や胃酸の状態の下剤として使用されています。ただし、下痢や嘔吐の発生によって明らかにされている - その有害な副作用はその使用を制限しています。また、消化管に損傷を与える可能性があります.
骨組織の修復におけるリン酸マグネシウムの使用は現在調査されており、Mg(H)の適用を調査している2PO4)2 セメントとして.
この形態のリン酸マグネシウムはこれに対する要求を満たす:それは生分解性で組織適合性である。加えて、骨組織の再生におけるその使用は、その強度および迅速な硬化のために推奨される。.
生分解性で非発熱性の整形外科用セメントとしての非晶質リン酸マグネシウム(AMP)の使用が評価されている。このセメントを生成するには、パテを形成するために、AMP粉末をポリビニルアルコールと混合します。.
リン酸マグネシウムの主な機能は、Mgの生物への貢献を提供することです。この元素は触媒または中間体として多くの酵素反応に介在し、生命に欠かせないものです。.
ヒトにおけるMgの欠乏は以下の効果と関連している:Caレベルの減少、心不全、Na保持、Kレベルの減少、不整脈、持続的な筋収縮、嘔吐、悪心、低循環副甲状腺ホルモン、胃および月経痛など.
参考文献
- SuSanA事務局(2010年12月17日)。顕微鏡下でストルバイト。 2018年4月17日、flickr.comから取得。
- 鉱物データ公開(2001-2005)。ボビエライト2018年4月17日、handbookofmineralogy.orgから取得
- Ying Yu、Chao Xu、Honglian Dai。分解性リン酸マグネシウム骨セメントの調製とキャラクタリゼーション, 再生バイオマテリアル, 第3巻、第4号、2016年12月1日、Pages 231-237、doi.org
- Sahar Mousa (2010)。りん酸マグネシウム材料の合成に関する研究りん研究速報Vol.24、pp 16-21.
- スモークフット(2018年3月28日)。 EntryWithCollCode38260。 [図データ] 2018年4月17日、commons.wikimedia.orgから取得しました。
- ウィキペディア(2018)。三塩基性リン酸マグネシウム。 2018年4月17日、en.wikipedia.orgから取得。
- パブケム(2018)。無水リン酸マグネシウム2018年4月17日、pubchem.ncbi.nlm.nih.govから取得
- Ben Hamed、T.、Boukhris、A.、Badri、A.、およびBen Amara、M.(2017)。新しいりん酸マグネシウムNa 3 RbMg 7(PO 4)6の合成と結晶構造Acta CrystallographicaセクションE:Crystallographic Communications、73(Pt 6)、817〜820。 doi.org
- バービー、E。、リン、B、ゴエル、V。非晶質リン酸マグネシウム(AMP)ベースの非発熱性整形外科用セメントの評価。バイオメディカルマット。第11巻(5):055010.
- ゆう、Y。、ゆう、CH。およびDai、H.(2016)。分解性マグネシウム骨セメントの調製再生バイオマテリアル第4巻(1):231


