水素化ナトリウム(NaH)の性質、反応性、危険性と使用
の 水素化ナトリウム は、式NaHの無機化合物である。それはナトリウムと水素化物との間にイオン結合を有する。その構造は図1に示されています。これは塩水和物の代表的なものです。これは、ボラン、メタン、アンモニアなどのより分子的な水素化物とは対照的に、Na +とH - イオンからなる塩に似た水素化物です。そして水.
結晶構造は配位数6を有し、各ナトリウム分子は八面体形状を有する8個の水素化物イオンによって囲まれており、図2に示されている(Mark Winter [The University of Sheffield and WebElements Ltd、1993-2016])。.
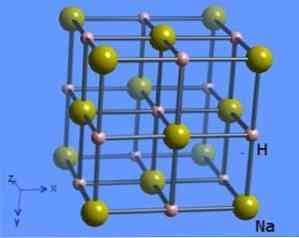
この化合物は、ナトリウムガスと水素ガスとの間の直接反応によって製造される(水素化ナトリウム配合 - 水素化ナトリウム用途、特性、構造および配合、2005-2017)。
H2 + 2Na→2NaH
水素化ナトリウムは、安全な取り扱いのために鉱油中60%w / wの分散形態(重量対重量%)として市販されている(SODIUM HYDRIDE、s.f.)。.
索引
- 1水素化ナトリウムの理化学的性質
- 2反応性と危険性
- 3つの用途
- 4参考文献
水素化ナトリウムの物理的および化学的性質
水素化ナトリウムは、一般に灰色または銀色で得られるが、純粋である場合には白色の固体である。その外観は図3に示されています.

NaHは、23.99771g / molの分子量、1.396g / mlの密度、および800℃の融点を有する(Royal Society of Chemistry、2015)。それは、アンモニア、ベンゼン、四塩化炭素および二硫化炭素に不溶である(国立バイオテクノロジー情報センター、s.f.)。.
化合物は非常に不安定です。純粋なNaHは空気中で容易に発火する可能性があります。空気中に存在する水と接触すると、引火性の高い水素を放出します。.
空気や湿気にさらされると、NaHは次の反応に従って水酸化ナトリウム(NaOH)の強い腐食性塩基に容易に加水分解されます。
NaH + H 2 O→NaOH + H 2
この反応では、水素化ナトリウムが塩基のように振舞うことが観察され得る。これは電気陰性度によるものです.
ナトリウムは水素(≒2.1)よりも著しく低い電気陰性度(≒1.0)を持っています。つまり、水素はナトリウムから離れてナトリウムから陽イオンと陰イオンを生成するために電子密度をそれ自身の方へ引き出します。水素化物の.
化合物がブレンステッド酸であるためには、水素から電子密度を分離する、すなわち酸素、フッ素、窒素などのような電気陰性原子にそれを結合する必要がある。そうして初めて、それは正式にはH +と表現され、それ自体は解離されるのです。.
水素化物は、H - としてよりよく説明され、自由電子対を有する。それ自体、ブレンステッド塩基であり、酸ではありません。実際、ルイスのようにブレンステッド酸/塩基の定義を拡張すれば、ナトリウム(Na +)がここでの酸種であるという結論に達するでしょう。.
H−塩基とH +酸とのブレンステッド酸/塩基反応生成物はH 2になる。酸性の水素は水から直接抽出されるので、反応が熱力学的に有利ではないとしても、水素ガスは泡立ち、平衡を置き換えます。.
水酸化ナトリウムを得るために、残りのNa +カチオンと一緒に書くことができるOH-イオンを残すことができる(水と反応した場合、なぜ固体の水素化ナトリウムがベースであり、酸性ではないのか、2016.
反応性と危険性
この化合物は強力な還元剤です。ガラス中のSiO2を攻撃する。特に水分の存在下で、気体のF2、Cl2、Br2およびI2(後者は100℃を超える温度で)と接触すると発火し、HF、HCl、HBrおよびHIを形成する。.
硫黄と反応してNa 2 SおよびH 2 Sを生成する。それはジメチルスルホキシドと爆発的に反応することがある。 -60℃でもアセチレンと激しく反応する。フッ素の中で自然に引火性.
それはエチル−2,2,3−トリフルオロプロピオネート中で重合反応を開始し、その結果エステルは激しく分解する。コハク酸ジエチルとトリフルオロ酢酸エチルの反応中の存在は爆発を引き起こした(SODIUM HYDRIDE、2016).
水素化ナトリウムは、水との反応による苛性副生成物の可能性があるため、皮膚または眼を腐食すると考えられています。.
目に入った場合は、まぶたの下で少なくとも15分間大量の水で洗い流し、直ちに医師の診察を受けてください。.
皮膚に触れた場合は、直ちにブラシをかけて患部を水で洗い流してください。刺激が続く場合は医師の診断を受ける。.
水への反応による摂取により有害です。嘔吐を誘発しないでください。直ちに医師の診察を受け、被害者を医療センターに転送する必要があります。.
水素化ナトリウムの油中分散は粉塵ではありません。ただし、反応する物質は細かい苛性ミストを放出することがあります。吸入した場合は、口を水で洗い流して空気の新鮮な場所に移してください。医師の診察を受けるべきである(Rhom and Hass Inc.、2007).
用途
水素化ナトリウムの主な用途は、(塩基によって触媒された)カルバニオンの形成を介して発生する縮合およびアルキル化反応を実施することです。.
油中の水素化ナトリウムは、アセト酢酸エステル、Claisen、Stobbe、Dieckmannおよび他の関連反応において脱プロトン化剤として機能する能力において、ナトリウムおよびナトリウム金属アルコラートに似ている。以下の点で他の縮合剤よりも優れています。
- それはより直接的な脱プロトン化をもたらす、より強い基盤です。.
- 過剰は必要ありません.
- 生成したH2は反応の程度の尺度を与える.
- 還元などの二次反応が排除される.
2−アミノピリジンおよびフェノチアジンのような芳香族および複素環式アミンのアルキル化は、トルエン - メチルホルムアミドの混合物を用いて高収率で容易に達成される。ジメチルホルムアミドの濃度は反応速度を制御するために使用される変数である(HINCKLEY、1957).
燃料電池自動車に使用するための水素貯蔵用の水素化ナトリウムの使用が提案されており、水素化物を放出するために水の存在下で粉砕されるプラスチック顆粒に封入されている。.
参考文献
- HINCKLEY、M.D.(1957)。水素化ナトリウムの製造、取扱い、および使用Advances in Chemistry、19巻、106〜117ページ.
- マークウィンター[シェフィールド大学およびウェブエレメンツリミテッド、U。ナトリウム:水素化ナトリウム。 WebElementsから取得しました:webelements.com.
- 国立バイオテクノロジー情報センター(S.F.)。 PubChem化合物データベース。 CID = 24758。 PubChemから取得:pubchem.ncbi.nlm.nih.gov.
- ロームアンドハス株式会社(2007年12月)水素化ナトリウム60%油中分散dow.comから取得.
- 化学の王立協会。 (2015)水素化ナトリウムChemSpiderから取得しました:chemspider.com.
- 水素化ナトリウム。 (2016) cameochemicalsから取得しました:cameochemicals.noaa.gov.
- 水素化ナトリウム配合 - 水素化ナトリウム用途、特性、構造および配合。 (2005-2017)。 Softschools.comから取得されました:softschools.com.
- 水素化ナトリウム。 (S.F.)。 chemicalland21から取得:chemicalland21.com.
- 水と反応させると固体の水素化ナトリウムをベースとし、酸性ではないのはなぜですか。 (2016年4月20日)。 stackexchangeから取得しました:chemistry.stackexchange.com.


