水酸化ストロンチウム(Sr(OH)2)の化学構造、性質および用途
の 水酸化ストロンチウム (Sr(OH)2)はストロンチウムイオン(Sr)と2つの水酸化物(OH)イオンからなる無機化合物である。この化合物はストロンチウム塩と強塩基を組み合わせて得られ、その化学式がSr(OH)であるアルカリ性の化合物をもたらします。2.
一般に、水酸化ストロンチウムを製造するための強塩基としては、水酸化ナトリウム(NaOH)または水酸化カリウム(KOH)が使用される。他方、強塩基と反応するストロンチウム塩(またはストロンチウムイオン)は硝酸ストロンチウムSr(NO)である。3)2 そしてプロセスは次の化学反応によって記述されます:
2KOH + Sr(NO3)2 →2KNO3 + Sr(OH)2
溶液中ではストロンチウムカチオン(Sr+)を水酸化物アニオン(OH)と接触させる。-)ストロンチウムの塩基性イオン塩を形成する。ストロンチウムはアルカリ土類金属なので、水酸化ストロンチウムは苛性アルカリ化合物と見なされます。.
索引
- 1入手
- 2化学構造と物理化学的性質
- 2.1水酸化ストロンチウム八水和物
- 2.2水酸化ストロンチウム一水和物
- 2.3無水水酸化ストロンチウム
- 2.4溶解度
- 2.5化学反応性
- 3つの用途
- 3.1糖蜜の抽出とてん菜の精製
- 3.2ストロンチウム脂肪
- 3.3プラスチック安定剤
- 3.4その他の用途
- 4参考文献
入手
先に説明した方法に加えて、一旦反応が行われると、Sr(OH)と言うことができる。2 溶液中に沈殿する。それからそれは洗浄と乾燥プロセスにかけられ、最終的に非常に細かい白い粉を得ます.
水酸化ストロンチウムを得るための代替方法は、炭酸ストロンチウム(SrCO)の加熱からのものである。3)または硫酸ストロンチウム(SrSO)4)500℃から600℃の間の温度の蒸気を用いて)。化学反応は以下のように起こります。
SrCO3 + H2O→Sr(OH)2 + CO2
SrS + 2H2O→Sr(OH)2 + H2S
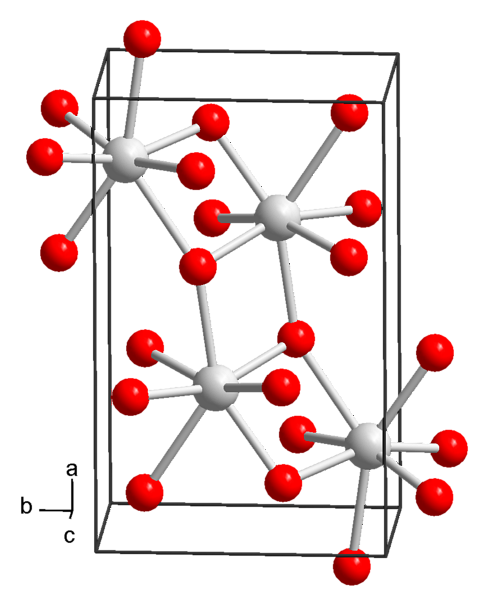
化学構造と物理化学的性質
現在、水酸化ストロンチウムの3つの形態が知られている:八水和物、一水和物および無水物。.
水酸化ストロンチウム八水和物
通常の温度と圧力の条件下(25℃、1気圧)の溶液から、水酸化ストロンチウムは八水和の形で沈殿します。その化学式はSr(OH)です。2∙8H2○.
この化合物は、265.76g / molのモル質量、1.90g / cm 2の密度を有し、そして四角形および無色のプリズム状外観の正方晶(空間群P4 / nccを有する)として沈殿する。.
また、水酸化ストロンチウム八水和物は、容易に潮解する化合物であるため、大気中の水分を吸収する能力を有する。.
水酸化ストロンチウム一水和物
光学顕微鏡検査(X線回折の手法を用いて行われる)によると、温度を約210℃に上げることによって - 一定の大気圧で - Sr(OH)2∙8H2あるいは脱水して水酸化ストロンチウム一水和物(Sr(OH))に変換する2∙H2O).
この形態の化合物は、139.65g / molのモル質量を有し、そしてその融解温度は、-73.15℃(375K)である。その原子構造のために、それは、その八水和形態で記載されたものよりも低い水への溶解度を示す。.
無水水酸化ストロンチウム
系の温度を約480℃まで上昇させ続けることによって、無水水酸化ストロンチウムが得られるまで脱水を続ける。.
その水和形態とは異なり、それは121.63 g / molのモル質量および3.625 g / cmの密度を有する。3. その沸点は710℃(1,310°Fまたは983K)であり、融点は535℃(995°Fまたは808K)です。.
溶解度
ストロンチウムの八水和水酸化物は、100ミリリットル当たり0.91グラムの水への溶解度(0℃で測定)を有するが、同様の温度条件でのその無水形態は、100ミリリットル当たり0.41グラムの溶解度を有する。.
同様に、この物質はアセトンに不溶、酸および塩化アンモニウムに完全に可溶であると考えられています。.
化学反応性
水酸化ストロンチウムは可燃性ではなく、その化学反応性は適度な温度と圧力で安定したままであり、大気中の二酸化炭素を吸収して炭酸ストロンチウムに変えることができます。.
さらに、それが皮膚、気道または体の他の粘膜領域と接触すると、非常に刺激性の高い化合物です。.
用途
その吸湿性の特徴と基本的な性質のために、水酸化ストロンチウムは業界の様々な用途に使用されています。
- ビートからの糖蜜の抽出と砂糖の精製.
- プラスチック安定剤.
- グリースと潤滑剤.
糖蜜の抽出とてん菜の精製
21世紀の初めに、1882年にCarl Scheiblerが特許を取得したプロセスによってビートから砂糖を精製するために、水酸化ストロンチウムがドイツで使用されました。.
この方法は、水酸化ストロンチウムとビートの糖パルプを混合することからなり、それは不溶性二糖をもたらす。この溶液はデカンテーションによって分離され、精製プロセスが実行されると、最終製品として砂糖が得られます。.
この手順は今日でも使用されていますが、より安価で、世界中の製糖所の大多数で使用されているため、はるかに需要の高い他の方法があります。例えば、珪酸バリウムを使用するBarsil法や、Calを抽出剤として使用するsteffen法.
ストロンチウムグリース
それらは水酸化ストロンチウムを含む潤滑グリースです。これらは金属特性を持つ表面に強く付着することができ、水に耐性がありそして温度の急激な変化に耐える.
その優れた物理的および化学的安定性により、これらの脂肪は工業用潤滑剤として使用されています。.
プラスチック安定剤
プラスチックの大部分は、太陽、雨、大気中の酸素などの気候要因にさらされると、その性質や劣化を変えます。.
かなりの耐水性のために、水酸化ストロンチウムはこれらのポリマーに添加されます - 融合段階の間 - プラスチック製品の製造における安定剤としてそれらの耐用年数を延ばすために作用します.
その他の用途
- 塗料業界では、商業用および工業用塗料の乾燥プロセスを促進するための必須添加剤として使用されています。.
- ストロンチウム塩またはストロンチウムイオンは水酸化ストロンチウムから得られそして火工品の製造のための原料として使用される。.
参考文献
- ウィキペディア(名詞)。水酸化ストロンチウムen.wikipedia.orgから取得しました
- PubChem。 (S.F.)。水酸化ストロンチウム。 pubchem.ncbi.nlm.nih.govから取得
- Lambert、I. and Clever、H. L.(2013)。水および水溶液中のアルカリ土類水酸化物books.google.co.veから取得
- Krebs、R. E.(2006)。私たちの地球の化学元素の歴史と使用:リファレンスガイド。 books.google.co.veから取得
- ハネウェル(S.F.)。水酸化ストロンチウム八水和物。 honeywell.comから回収


