特徴的な無極性分子、それらを識別する方法および例
の 無極性分子 それらはそれらの構造中にそれらの電子の対称的分布を示すものである。これは、その原子の電気陰性度の差が小さい場合、または電気陰性の原子または基が分子内でそれらの効果を打ち消す場合に可能です。.
常に「無極性」が絶対というわけではありません。このため、極性極性分子は無極性と見なされることがあります。すなわち、それは0に近い双極子モーメントμを持ちます。ここでは相対の地形を入力します。?
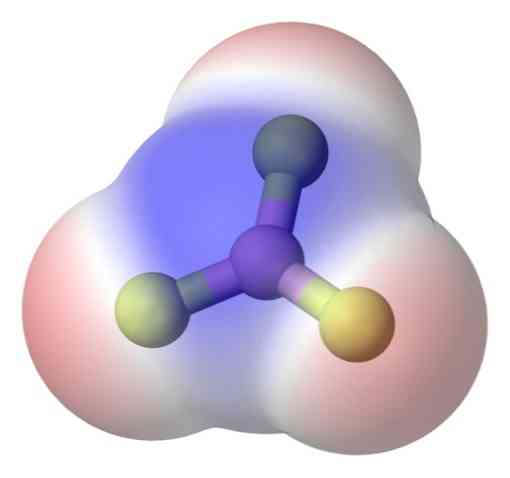
この問題をよりよく解決するために、三フッ化ホウ素分子BFがあります。3 (トップ画像).
フッ素原子はホウ素原子よりもはるかに電気陰性度が高いため、B-F結合は極性があります。しかし、BF分子3 対称(三角平面)で、3つのモーメントB-Fのベクトル相殺を含みます。.
したがって、極性結合が存在しても、無極性分子も生成される。生成された極性は、前のリンクと同じ大きさであるが反対方向を向いている別の極性リンクの存在によってバランスをとることができる。 BFで起こるように3.
索引
- 1無極性分子の特徴
- 1.1対称性
- 1.2電気陰性度
- 1.3分子間力
- 2それらを識別する方法?
- 3例
- 3.1希ガス
- 3.2二原子分子
- 3.3炭化水素
- 3.4その他
- 4参考文献
無極性分子の特性
対称性
極性結合の効果が互いに打ち消し合うためには、分子は特定の幾何学的構造を持たなければならない。例えば、線形、一目で最もわかりやすい.
これは二酸化炭素(CO)の場合です2これは2つの極性リンクを持っています(O = C = O)。これは、C = Oリンクの2つの双極子モーメントが180°の角度で一方の側に向かい、もう一方の側に向いているときに互いに打ち消し合うという事実によります.
したがって、分子の「無極性」を鳥瞰図として評価するときに考慮する最初の特性の1つは、それがいかに対称的であるかを観察することです。.
COではなく2 カルボニルスルフィドと呼ばれるCOS分子(O = C = S)があります。.
硫黄の電気陰性度は酸素の電気陰性度より小さいので、今やそれはもはや無極性分子ではない。したがって、双極子モーメントC = SはC = Oのそれとは異なります。結果として、COSは極性分子です(極性は他の袋からの粉です)。.
下の図は、これまで説明してきたことをすべてグラフィック形式で要約したものです。
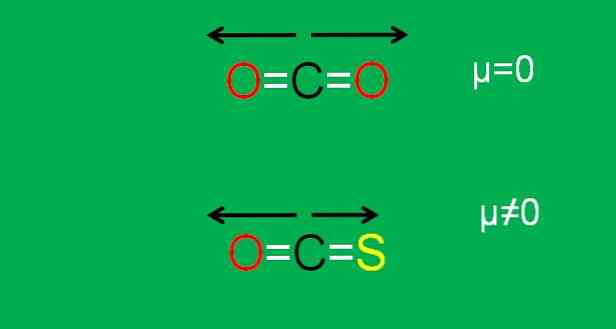
C = S結合の双極子モーメントは、COS分子のC = O結合の双極子モーメントよりも小さいことに注意してください。.
電気陰性度
ポーリング尺度の電気陰性度は、0.65(フランの場合)から4.0(フッ素の場合)までの値です。一般に、ハロゲンは高い電気陰性度を有する。.
共有結合を形成する元素の電気陰性度の差が0.4以下である場合、それは無極性または無極性であると言われる。しかし、本当に無極性の唯一の分子は、同一の原子間の結合によって形成されたものです(水素、H-Hなど)。.
分子間力
物質が水に溶けるためには、分子と静電的に相互作用しなければなりません。無極性分子が作ることができない相互作用.
無極性分子では、それらの電荷は分子の一端に閉じ込められているのではなく、対称的に(または均一に)分布している。したがって、双極子 - 双極子力を介して相互作用することはできません.
対照的に、無極性分子はロンドンの分散力を介して互いに相互作用します。これらは、隣接分子の原子の電子雲を分極させる瞬間双極子です。ここで分子量はこれらの分子の物理的性質における主な要因です。.
それらを識別する方法?
-無極性分子を同定するためのおそらく最も良い方法の1つは異なる極性溶媒へのその溶解度であり、一般にそれらにはほとんど溶けない。.
-一般に、無極性分子は事実上気体である。それらは水と混ざらない液体を形成することもあります。.
-無極性固体は柔らかいという特徴があります.
-それらをまとめる分散力は一般に弱い。このため、それらの融点または沸点は極性の性質の化合物のそれらより低い傾向があります.
-特に液体形態の無極性分子は、正味電荷を欠いているため、電気の伝導性が低い.
例
希ガス
それらは分子ではありませんが、希ガスは無極性と見なされます。 2つの短い期間、その原子のうちの2つが相互作用すると仮定すると(He-He)、この相互作用は分子と見なすことができます(半分)。本来無極性になる分子.
二原子分子
Hなどの二原子分子2, Br2, 私は2, Cl2, O2, そしてF2, それらは無極性です。これらは一般式Aとして2, A-A.
炭化水素
もしAが原子団だったら?それは他の無極性化合物の前にあるでしょう。例えば、エタン、CH3-CH3, 炭素骨格が線状であるもの、C-C.
メタン、CH4, とエタン、C2H6, それらは無極性分子です。カーボンの電気陰性度は2.55です。水素の電気陰性度は2.2です。それゆえ、水素から炭素へ配向した低強度双極子ベクトルがある。.
しかし、メタンとエタン分子の幾何学的対称性のため、それらの分子の双極子ベクトルまたは双極子モーメントの合計はゼロであるため、分子には正味の電荷はありません。.
一般に、すべての炭化水素に同じことが起こり、それらに不飽和(二重および三重結合)がある場合でも、それらは無極性または低極性化合物と見なされます。同様に、環状炭化水素はシクロヘキサンまたはシクロブタンなどの無極性分子である。.
その他
二酸化炭素(CO)の分子2)および二硫化炭素(CS)2)無極性分子であり、両方とも線形形状を有する。.
二硫化炭素において、炭素の電気陰性度は2.55であり、一方硫黄の電気陰性度は2.58である。両方の要素が実質的に同じ電気陰性度を持つように。双極子ベクトルは生成されないため、正味電荷はゼロです。.
また、以下のCCl分子があります。4 とAlBr3, 両極性:
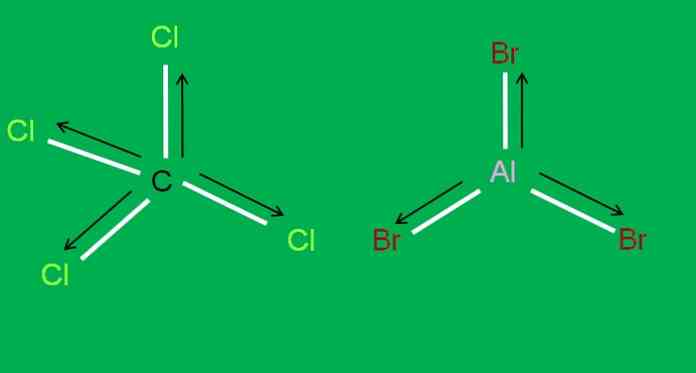
三臭化アルミニウムでは、AlBr3 それはBFと同じように起こります3, 記事の始めに。一方、四塩化炭素については、CCl4, すべてのC-Cl結合が等しいので、幾何学は四面体で対称です。.
同様に、一般式CXを有する分子4 (CF4, CI4 とCBr4)、彼らはまた無極性です.
そして最後に、無極性分子は、六フッ化硫黄、SFの場合のように、八面体形状さえも有することができる。6. 実際、それは対称的であり、その電子分布が均一である限り、それは任意の幾何学形状または構造を有することができる。.
参考文献
- Carey F. A.(2008)。有機化学カルボン酸(第6版)。マックグローヒル.
- CedrónJ.、Landa V.、Robles J.(2011)。分子の極性取得元:corinto.pucp.edu.pe
- チューターVista (2018)。非極性分子以下から取得しました:chemistry.tutorvista.com
- Helmenstine、Anne Marie、Ph.D. (2019年1月28日)極性および非極性分子の例以下から取得しました:thoughtco.com
- Kurtus R.(2016年9月19日)極性および非極性分子チャンピオンのための学校。取得元:school-for-champions.com
- Ganong W.(2004)。医学生理学エディション19ª. 現代マニュアルの社説.


