浸透圧公式、それを計算する方法および浸透圧との差
の 浸透圧 それは、前記溶液の浸透圧として知られる併合特性に寄与する限り、溶液1リットル中の化合物の濃度を測定するパラメータである。.
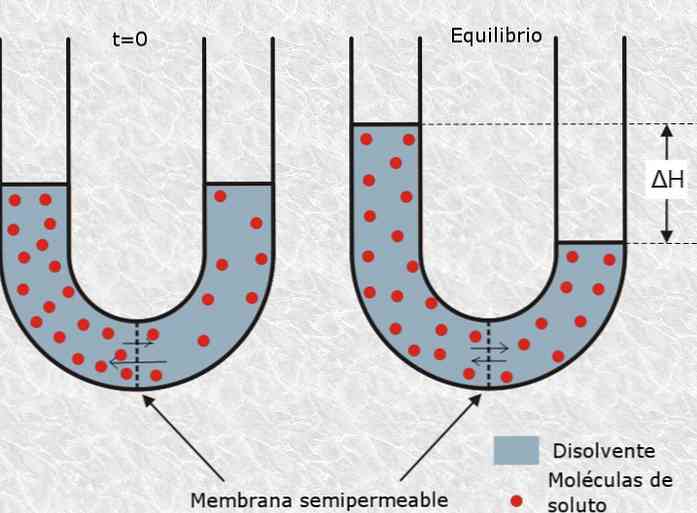
この意味で、溶液の浸透圧は、浸透プロセスを遅くするのに必要な圧力の量を指し、これは溶液からの半透膜または多孔質膜による溶媒粒子の選択的通過として定義される。低濃度から高濃度へ.
また、溶質粒子の量を表すのに使用される単位はオスモル(その記号はOsm)であり、これはほとんど全世界で使用されている国際単位系(SI)の一部ではありません。そのため、溶液中の溶質の濃度は、1リットル当たりのオスモル数(Osm / l)の単位で定義されます。.
索引
- 1式
- 1.1モル浸透圧濃度公式の変数の定義
- 2計算方法?
- 3浸透圧と浸透圧の違い
- 4参考文献
式
前述のように、浸透圧(浸透圧濃度としても知られている)は、Osm / lとして定義される単位で表される。これは、浸透圧の決定および浸透による溶媒拡散の測定とのその関係によるものである。.
実際には、浸透圧濃度は浸透圧計を用いて物理量として決定することができる。.
浸透圧計は、値を得るために溶液の浸透圧の測定、およびその他の併合的性質(蒸気圧、沸点上昇または凝固点降下など)の決定に使用される機器です。溶液のモル浸透圧濃度.
このようにして、この測定パラメータを計算するために、この特性に影響を及ぼし得る全ての要因を考慮に入れる以下の式が使用される。.
浸透圧=Σφ私はn私はC私は
この式では、浸透圧モル濃度は、3つの異なるパラメータから得られるすべての値を掛け合わせることによって得られる合計として確立されます。.
モル浸透圧濃度の式における変数の定義
1つ目は、ギリシャ文字のφ(phi)で表される浸透係数です。これは、理想的な振る舞いの解がどれだけ遠ざかっているか、つまり溶質が解に現れる非理想性の程度を説明します。.
最も簡単には、φは溶質の解離度を意味し、これは0から1の間の値をとることができ、単位の最大値は100%の解離を表す。つまり、絶対的な.
スクロースのようないくつかのケースでは、この値は1を超えます。一方、塩の場合のように、絶対的な解離が起こったとしても、静電相互作用や力の影響により、1未満の値の浸透係数が生じる。.
一方、nの値は、分子が解離し得る粒子の量を示す。イオン種の場合、nの値が2に等しい塩化ナトリウム(NaCl)が例として挙げられる。非イオン化グルコース分子では、nの値は1に等しい.
最後に、cの値は溶質の濃度を表し、モル単位で表されます。下付き文字iは特定の溶質の同一性を表しますが、上記の3つの因子を掛け合わせて浸透圧を求めるときも同じでなければなりません。.
それを計算する方法?
イオン性化合物KBr(臭化カリウムとして知られている)の場合、水中に1 mol / lのKBrに等しい濃度の溶液があれば、それは2 osmol / lに等しいモル浸透圧濃度を持つと推論される。.
これは、その強い電解質の性質によるもので、水中での完全な解離を促進し、2つの独立したイオンの放出を可能にします(K+ とBr-それはいくらかの電荷を持っているので、KBrの各モルは溶液中で2オスモルに等しい.
同様に、1mol / lのBaClに等しい濃度の溶液についても同様である。2 水中で(塩化バリウムとして知られている)、それは3オスモル/ lに等しいオスモル濃度を有する。.
これは、3つの独立したイオンが放出されるためです。Baイオン2+ そして2つのClイオン-. その後、各モルのBaCl2 解の3オスモルに相当する.
他方、非イオン種はそのような解離を受けず、溶質1モルにつき単一オスモルを生じる。 1mol / lに等しい濃度のグルコース溶液の場合、これは1lsmol / l溶液のlに等しい。.
浸透圧と浸透圧の違い
オスモルは、22.4リットルの溶媒に等しい体積に溶解され、0℃の温度にさらされ、そして1気圧に等しい浸透圧の発生を引き起こす粒子の数として定義される。これらの粒子は浸透圧的に活性であると考えられることに注意すべきである。.
この意味で、浸透圧と浸透圧として知られる特性は同じ測定値を指します。つまり、溶液中の溶質の濃度、言い換えれば、溶液中の溶質の全粒子の含有量です。.
浸透圧と浸透圧の間に確立される基本的な違いは、それぞれが表される単位にあります。
重量オスモル濃度は、溶液の体積当たりの物質の量(すなわち、オスモル/リットル)で表され、一方、モル浸透圧濃度は、溶媒の質量当たりの物質の量(すなわち、オスモル/ kg溶液)で表される。.
実際には、異なる測定値の合計の大きさの間に認識できない差があるという事実のために、両方のパラメータは異なる単位で現れても無関係に使用されます。.
参考文献
- ウィキペディア(S.F.)。浸透圧濃度es.wikipedia.orgから取得しました
- Chang、R.(2007)。化学、第9版。メキシコ:McGraw-Hill.
- Evans、D. H.(2008)。浸透圧およびイオン調節細胞と動物books.google.co.veから取得
- Potts、W. T.、and Parry、W.(2016)。動物における浸透圧およびイオン調節books.google.co.veから取得
- Armitage、K.(2012)。一般生物学における調査books.google.co.veから取得


