硫酸アルミニウム(Al 2(SO 4)3)の構造、用途、種類、毒性
の 硫酸アルミニウム 式Alの無機アルミニウム塩である。2(SO4)3, それは通常光沢のある結晶を持つ白い固体として表示されます。化合物の色は、その鉄の濃度およびその他の不純物の影響を受けます。硫酸アルミニウムには主に2つのタイプがあります:AとB.
下の画像では、硫酸アルミニウム水和物の白い結晶が示されています。結晶格子内の鉄イオンを示す茶色の着色がないことは注目に値する。.

硫酸アルミニウムは水に非常に溶けやすい塩であり、本来無水の形で見つけることは稀です。それは通常八水和物の硫酸アルミニウムの形で水和されている[Al2(SO4)3.18時間2O]または16水和物[Al]2(SO4)3.16H2O].
同様に、それは、ミョウバンとして知られている化合物、カリウムおよびアンモニウムと複塩を形成することができる。部分的には、これはアルミニウム以外の他のイオンを保持するための水和物内の水の親和性によるものであり得る。.
硫酸アルミニウムは、水酸化アルミニウムおよび硫酸中の水の作用によって分解することがある。この特性は土の酸性化剤としてそれの使用を可能にしました.
それはまた特に粉との接触によって有毒な混合物です。しかしながら、それは、凝固の方法による水の浄化から、治療目的でのその使用まで、いくつかの産業での使用を通して起こる無限の用途および用途を有する。.
索引
- 1つの構造
- 2それは何のためにあるのか(用途)
- 2.1水の凝固または凝集
- 2.2インクの媒染剤として、そして紙の精巧さの中での使用
- 2.3産業用
- 2.4薬用および治療用
- 2.5その他の用途
- 3硫酸アルミニウムの製造
- 4種類
- 5毒性
- 6参考文献
構造
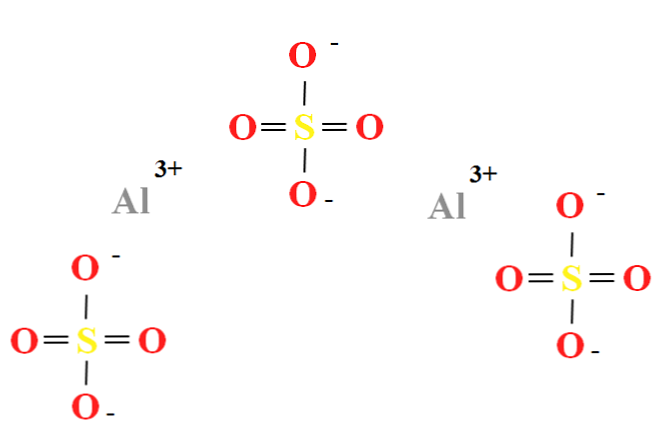
硫酸アルミニウムは、2つのAlカチオンの比率を有する。3+ 陰イオン3個ごと42- (上の画像)、化学式Alで直接観察できます2(SO4)3.
Alに注意してください3+ 彼らは灰色がかっている42- それらは黄色(硫黄原子用)と赤(酸素原子用)です。.
図示の構造は、無水形態のAlに対応する。2(SO4)3, 水分子はイオンと相互作用しないからである。あなたの水和物では、しかし、水はアルのポジティブセンターに引き付けることができます3+, または負のSO四面体による42- 水素結合を介して(HOH-O-SO)32-).
アル2(SO4)3∙18H2あるいは、例えば、それはその固体構造中に18個の水分子を含む。それらのいくつかはAlと直接接触しているかもしれません3+ またはSOと42-. 言い換えれば:硫酸アルミニウムは、内部または外部配位水を持つことができます.
また、その構造はFeのような他の陽イオンを収容することができます。3+, な+, K+, 等しかしこれのために、それはそれ以上の陰イオンの存在が必要です42-. 何のため?金属不純物による正電荷の増加を中和する.
硫酸アルミニウムは多くの構造を持つことができますが、その水和物は単斜晶系を採用する傾向があります.
物理的および化学的性質
外観
それは光沢のある白い結晶、顆粒または粉末で固体として見えます.
分子量
342.31 g / mol(無水).
匂い
無臭です
味
適度に収まる甘い味.
融点
770℃無水形(86.5℃オクタデカヒドラタダ形)
水への溶解度
0℃で31.2g / 100ml。 20℃で36.4 g / 100 ml、100℃で89 g / 100 ml.
密度
2.67〜2.71 g / cm3.
溶解度
エチルアルコールにやや溶ける.
蒸気圧
基本的にゼロ.
安定性
空気中で安定.
分解
加熱すると、ほぼその融点で、それは特に硫黄酸化物、有毒ガスを放出することによって分解することができる.
腐食性
硫酸アルミニウム溶液はアルミニウムに対して腐食性です。また、湿気があると化合物が金属を腐食することがあります。.
pKa
3.3から3.6。そしてそのpHは5%水溶液中で2.9以上である。.
用途は何ですか
水の凝固または凝集
-水と混ぜると(飲用、使用済または廃棄)、硫酸アルミニウムは水酸化アルミニウムを生成し、溶液中の化合物および粒子と錯体を形成してそれらの沈降を促進します。長い時間.
-硫酸アルミニウムはスイミングプールの水の洗浄にも使用されているため、使用するのに魅力的です。.
-硫酸アルミニウムの使用を通して、水は濁りおよび色なしで得られ、水の洗浄を容易にすることによってその飲用性を高める。残念ながら、この浄化方法では水中のアルミニウム濃度がわずかに上昇する可能性があります。.
-アルミニウムは、皮膚、脳、肺に蓄積する非常に有毒な金属であり、深刻な障害を引き起こします。また、それが生き物の中でどのような機能を果たしているのかはわかりません。.
-欧州連合は、水中のアルミニウムの最大許容限度が0.2 mg / Lを超えないことを要求しています。一方、米国環境保護局は、アルミニウムによる最大水汚染限度が0.05-0.2 mg / lを超えないことを要求しています.
-廃水の処理または硫酸アルミニウムとの併用により、経済的にそれらの中のリンの除去または削減が可能になります。.
インクの媒染剤として、そして紙の精巧さの中での使用
-硫酸アルミニウムは染料やインクの媒染剤として使われてきました。その固定作用はAl(OH)による3, そのゼラチン状の稠度が織物への染料の吸着に寄与する.
-記述された目的のために紀元前2000年頃から使われてきましたが、有機染料だけが媒染剤を必要とします。合成染料は、その一方で、その機能を果たすために媒染剤を必要としません.
-それは紙の製造から置き換えられていますが、それはまだ紙パルプの製造に使用されています。不純物を除去し、材料を結合し、電荷を中和し、ロジンを校正するために使用されてきた.
産業用として
-それはコンクリートの硬化を促進するために建設業界で使用されます。さらに、それは建物の防水に使用されています.
-石鹸および脂肪産業では、それはグリセリンの生産で使用されています.
-それは操作の間に使用される総合的な触媒の製造で石油産業で使用されます.
-医薬品や化粧品の製造における収斂剤として製薬業界で使用されています。.
-カルミンなどの染料の製造に介入する。それはブタジエンスチレンの合成ゴムの製造における染料としても使用される.
-製糖業界では、サトウキビの糖蜜精製剤として使用されています.
-消臭剤の製造に使用されています。なんで?それは汗腺の管の狭窄を引き起こし、かくして汗の蓄積を制限するので、匂いを引き起こす細菌の増殖に必要な培地です。.
-それは革のなめし、その使用に必要なプロセスで使用されています。さらに、それは肥料の製造に使用されています.
-それは、塗料、接着剤およびシーラント、ならびに家具用の洗浄剤および手入れ剤の製造における添加剤として使用されている。.
薬用および治療用
-硫酸アルミニウムは免疫学的アジュバントです。したがって、それは、それらの作用部位で放出されたときに、接種された抗原に対する抗体のより多くの産生を生じるように抗原を処理する機能を果たす。.
-フロイントアジュバントおよびBCG、ならびにインターロイキンなどの内因性アジュバントを含む他のアジュバントは、抗原に対して非特異的であり、免疫作用の範囲の拡大を可能にする。これは多くの病気に対するワクチンの開発を可能にしました.
-硫酸アルミニウムの凝固作用により、処理水中の多数のウイルス、特にQベータ、MS2、T4およびP1の除去が可能になりました。結果は、硫酸アルミニウムによる水の処理がそのようなウイルスの不活性化を生じることを示している。.
-硫酸アルミニウムは、髭剃り時に発生する小さな表面の傷や擦り傷の治療にスティックの形でまたは粉末として使用されます.
-それは酢酸アルミニウム、いくつかの耳の状態の治療に使用される化合物の製造に使用されます。それはまた、大きな成功を収めずに、抗蟻咬傷の結果を軽減するためにも使用されてきた。.
-硫酸アルミニウムの溶液は、5〜10%の濃度で、それらの分泌物の抑制を可能にする潰瘍の局所治療に使用されます.
-硫酸アルミニウムの収斂作用は、皮膚の表層を収縮させ、タンパク質を凝固させ、そして傷を癒します.
その他の用途
-硫酸アルミニウムは、池、湖、水の流れの中での藻類の過剰な繁殖の抑制を助けます。それはまた軟体動物、とりわけスペインのナメクジの除去にも使用されます。.
-庭師はアルカリ性土を酸性にするのにこの混合物を適用する。その水と接触すると、硫酸アルミニウムは水酸化アルミニウムと希硫酸に分解される。その後、水酸化アルミニウムが沈殿し、硫酸が溶液中に残る.
-硫酸による土壌の酸性化は、アジサイと呼ばれる植物が存在するために非常に独創的な方法で視覚化され、その花は酸性土壌の存在下で青くなります。つまり、それらは敏感で、pHの変化に反応します.
-硫酸アルミニウムは、火災と戦うためのフォームの製造に関与しています。どうですか?炭酸水素ナトリウムと反応してCOを放出する2. このガスはOアクセスをブロックします2 材料の燃焼部位へ。その結果、停滞していた停戦.
硫酸アルミニウムの製造
硫酸アルミニウムは、ボーキサイト鉱などのアルミニウムに富む化合物を硫酸と高温で反応させることによって合成される。次の化学式は反応を表します。
アル2○3 + H2そう4 ->アル2(SO4)3 + 3 H2○
硫酸アルミニウムは、次の反応に従って、水酸化アルミニウムと硫酸との中和反応によっても形成され得る。
2 Al(OH)3 + 3 H2そう4 + 12 H2O - > Al2(SO4)3.18時間2○
硫酸はアルミニウムと反応して硫酸アンモニウムを形成し、水素分子をガスの形で放出する。反応は次のように図式化されます。
2 Al + 3 H2そう4 ->アル2(SO4)3 + 3 H2
タイプ
硫酸アルミニウムは2つのタイプに分類されます:タイプAおよびタイプB。硫酸アルミニウムタイプAでは、固体は白で、0.5%未満の鉄濃度を持っています.
硫酸アルミニウムB型では、固形物は褐色であり、1.5%未満の鉄濃度を有する。.
硫酸アルミニウムを製造する産業には、分類の基準が異なります。かくして、産業はそのタイプA硫酸アルミニウムの製造について酸化鉄として最高濃度0.1%の鉄を報告している。タイプBの間それらは0.35%の最大鉄濃度を示します.
毒性
-硫酸アルミニウムはその粉塵と接触することによってその毒性作用を発揮し、それによって皮膚の炎症を引き起こし、そして接触が頻繁にある場合には皮膚炎を引き起こす化合物である。.
-目には強い苛立ちを引き起こし、永久的な怪我をすることさえあります。.
-吸入すると鼻やのどに刺激を与え、咳や発疹の原因になります。.
-その摂取は胃の刺激、悪心および嘔吐を引き起こします.
-直接硫酸アルミニウムによるものではないが、間接的にその使用によるものであるという毒性作用がある。これは、水の浄化に硫酸アルミニウムを使用することによって引き起こされる、アルミニウムの特定の毒性作用の場合です。.
-硫酸アルミニウムを使用して精製水で調製した塩を使用して慢性的に透析されている患者は、非常に深刻な健康障害を経験します。これらの疾患のうち、貧血、透析による認知症、骨疾患の増加があります。.
参考文献
- ウィキペディア(2018)。硫酸アルミニウム撮影元:en.wikipedia.org
- アリスインダストリアル硫酸アルミニウム溶液タイプAおよびB。撮影場所:aris.com.pe
- クリストファーボイド(2014年6月9日)硫酸アルミニウムの主な工業用途撮影者:chemservice.com
- PubChem。 (2018)。無水硫酸アルミニウム撮影者:pubchem.ncbi.nlm.nih.gov
- アンデシアケミカル(2009年8月20日)硫酸アルミニウムの安全シート[PDF]撮影元:andesia.com
- 化学書(2017)硫酸アルミニウム撮影者:chemicalbook.com


