エチルエーテルの性質、構造、入手方法、用途
の エチルエーテル, ジエチルエーテルとも呼ばれ、化学式がCの有機化合物です。4H10年それは無色で揮発性の液体であることを特徴としており、それ故に、その瓶はできるだけ気密に閉じて保たれなければならない。.
このエーテルはジアルキルエーテルの一員として分類される。すなわち、それらは式ROR 'を有し、ここでRおよびR'は異なる炭素セグメントを表す。そしてそれがその中間名、ジエチルエーテルを説明するように、酸素原子に結合する2つのラジカル - エチルである.

当初エチルエーテルは、1846年にWilliam Thomas Green Mortonによって紹介された全身麻酔薬として使用されました。しかしながら、その可燃性のために、その使用は拒絶され、それを他のより危険性の低い麻酔薬と置き換えた。.
この化合物は、患者の心血管状態の評価中に、血液循環の時間を推定するためにも使用されています.
体内では、ジエチルエーテルは二酸化炭素と代謝物に変換されます。後者は尿に排泄されることになります。しかし、投与されたエーテルのほとんどは、何の変更も受けずに肺で吐き出されます。.
一方、それは石鹸、オイル、香水、アルカロイドとガムのための溶媒として使われます.
索引
- 1エチルエーテルの構造
- 1.1分子間力
- 2物理的および化学的性質
- 2.1その他の名前
- 2.2分子式
- 2.3分子量
- 2.4外観
- 2.5匂い
- 2.6味
- 2.7沸点
- 2.8融点
- 2.9引火点
- 2.10水への溶解度
- 2.11他の液体への溶解度
- 2.12密度
- 2.13蒸気密度
- 2.14蒸気圧
- 2.15安定性
- 2.16オートイグニッション
- 2.17分解
- 2.18粘度
- 2.19燃焼熱
- 2.20気化熱
- 2.21表面張力
- 2.22イオン化ポテンシャル
- 2.23臭気閾値
- 2.24屈折率
- 3入手
- 3.1エチルアルコールから
- 3.2エチレンから
- 4毒性
- 5つの用途
- 5.1有機溶剤
- 5.2全身麻酔
- 5.3エーテルの精神
- 5.4血行の評価
- 5.5教育機関
- 6参考文献
エチルエーテルの構造
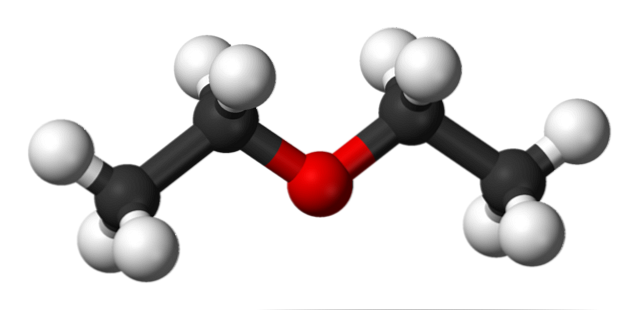
上の画像では、エチルエーテルの分子構造の球と棒のモデルによる表現があります。.
見て分かるように、酸素原子に対応する赤い球は、両側に結合した2つのエチル基を有する。すべてのリンクはシンプルで柔軟性があり、軸を中心に自由に回転できます。.
これらの回転は配座異性体として知られる立体異性体を起源とする。異性体よりも、それらは代替の空間的状態です。画像の構造は反立体配座異性体に正確に対応しており、そこではすべての原子群が互い違いになっています。.
他の配座異性体は何でしょうか?食い込み、そしてあなたの画像は利用できませんが、単にU字型でそれを視覚化しますUの上端にはメチル基があります。3, これは立体反発を経験するでしょう(それらは宇宙で衝突するでしょう).
したがって、CH分子は3CH2OCH2CH3 ほとんどの場合反立体配座を採用する.
分子間力
液相ではエチルエーテル分子はどのような分子間力で支配されているのでしょうか。それらの双極子モーメント(1.5D)は電子密度が十分に不十分な領域(δ+)を欠いているので、それらは主に分散力のおかげで液体中に維持される。
これは、エチル基の炭素原子が酸素原子に過剰な電子密度を与えないためである。上のことは手元のエチルエーテルの静電ポテンシャルのマップで明らかです(下の画像)。青い領域がないことに注意してください.
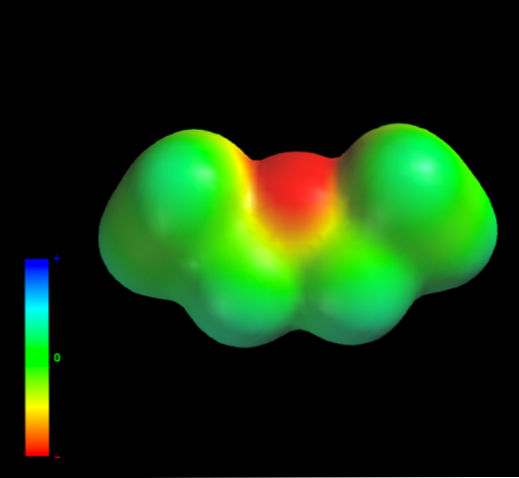
分子構造中に利用可能なO − H結合がないので、酸素もまた水素結合を形成することができない。それゆえ、それらの分散力を支持するのは瞬間双極子およびそれらの分子量である。.
それにもかかわらず、それは水に非常に溶けやすいです。なんで?酸素原子は電子密度が高いため、水分子から水素結合を受け取ることができるため、
(CH3CH2)2○δ- - δ+H-OH
これらの相互作用は100mLの水に溶ける6.04gのこのエーテルの原因です。.
物理的および化学的性質
その他の名前
-ジエチルエーテル
-エトキシエタン
-酸化エチル
分子式
C4H10年Oまたは(C2H5)2○.
分子量
74.14 g / mol.
外観
無色の液体.
匂い
甘くて辛い.
味
燃えて甘い.
沸点
94.3ºF(34.6ºC)〜760 mmHg.
融点
-177.3°F(-116.3°C)。安定した水晶.
発火点
-49ºF(密閉容器).
水への溶解度
25℃で6.04 g / 100 mL.
他の液体への溶解度
短鎖脂肪族アルコール、ベンゼン、クロロホルム、石油エーテル、脂肪溶媒、多くの油および濃塩酸と混和性.
アセトンに可溶で、エタノールに非常に可溶です。それはまたナフサ、ベンゼンおよびオイルに溶けます.
密度
68°F(20°C)で0.714 mg / mL.
蒸気密度
2.55(密度1の空気との関係で).
蒸気圧
68ºFで442 mmHg。 25℃で538mmHg。 20℃で58.6 kPa.
安定性
それは過酸化物の形成と空気、湿気および光の作用によってゆっくり酸化されます.
過酸化物の形成は、開封されて6ヶ月以上保管されているエーテル容器中で起こる可能性があります。過酸化物は、摩擦、衝撃、または加熱によって爆発する可能性があります。.
亜鉛、ハロゲン、非金属オキシハロゲン化物、強酸化剤、塩化クロミル、テメンチンオイル、硝酸塩、金属塩化物との接触を避けること。.
オートイグニッション
356ºF(180ºC).
分解
ウォームアップすると分解し、刺激性の刺激性の煙を発する。.
粘度
20℃で0.2448 cPoise.
燃焼熱
8,807 Kcal / g.
気化熱
30℃で89.8cal / g.
表面張力
20℃で17.06ダイン/ cm.
イオン化ポテンシャル
9.53 eV.
臭気閾値
0.83 ppm(純度は表示されていません).
屈折率
15℃で1,355.
入手
エチルアルコールから
エチルエーテルは、触媒としての硫酸の存在下で、エチルアルコールから得ることができる。水性媒体中の硫酸は解離してヒドロニウムイオンHを生成する。3○+.
無水エチルアルコールは硫酸溶液中を流れ、130℃と140℃の間に加熱され、エチルアルコール分子のプロトン化を生じる。続いて、非プロトン化エチルアルコールの他の分子がプロトン化分子と反応する。.
これが起こると、エチルアルコールの2番目の分子の求核攻撃により、最初の分子(プロトン化されたもの)からの水の放出が促進されます。その結果、プロトン化エチルエーテルが形成される(CH3CH2OHCH2CH3)部分的に帯電した酸素を含む.
しかしながら、この合成方法は、硫酸がプロセス中に生成された水(エチルアルコールの脱水の生成物)で希釈されるので効率を失う。.
反応温度は重要です。 130℃以下の温度では反応が遅く、ほとんどの場合エチルアルコールが蒸留されます。.
150℃を超えると、硫酸はエチルアルコールと結合してエチルエーテルを形成する代わりに、エチレン(二重結合アルケン)を形成します。.
エチレンから
反対の方法、すなわち気相中でのエチレンの水和では、エチルアルコールに加えてエチルエーテルが副生成物として形成され得る。実際、この合成経路はこの有機化合物の大部分を生成します。.
この方法は固体支持体に固定されたリン酸触媒を使用し、より多くのエーテルを生成するように調整することができる。.
アルミナ触媒の存在下でのエタノールの気相での脱水は、エチルエーテルの製造において95%の収率を与え得る。.
毒性
接触により皮膚や目に刺激を与える可能性があります。皮膚との接触は、その乾燥やひび割れを引き起こす可能性があります。それはすぐに蒸発するので、エーテルは通常皮膚を貫通しません.
エーテルによる眼の刺激は通常軽度であり、重度の刺激の場合、損傷は通常可逆的です。.
その摂取は麻薬作用と胃の刺激を引き起こします。激しい摂取は腎臓障害を引き起こす可能性があります.
エーテルを吸入すると、鼻やのどを刺激することがあります。エーテル吸入の場合:眠気、興奮、めまい、嘔吐、不規則な呼吸、唾液分泌の増加.
高曝露は意識の喪失や死さえも引き起こす可能性があります.
OSHAは、8時間シフト中に平均800 ppmの職業ばく露限度を設定する.
眼の刺激レベル:100 ppm(ヒト)。眼の刺激レベル:1200 mg / m3 (400 ppm).
用途
有機溶剤
それは臭素、ヨウ素および他のハロゲンを溶かすのに使用されるのは有機溶媒です。大部分の脂質(脂肪)、樹脂、純粋なゴム、いくつかのアルカロイド、ゴム、香水、酢酸セルロース、硝酸セルロース、炭化水素および染料.
さらに、それは動物の組織や植物の有効成分の抽出に使用されます。なぜなら、それは水よりも密度が低く、その上に浮遊していて、目的の物質をエーテルに溶解したままにするからです.
全身麻酔
それは1840年以来一般的な麻酔薬として使用されてきました。しかしながら、それは可燃性物質であり、そしてそれ故に、臨床環境内でのその使用のために深刻な困難に遭遇する。.
さらに、それは患者に悪心および嘔吐のようなある望ましくない術後の副作用をもたらします.
これらの理由から、一般的な麻酔薬としてのエーテルの使用は破棄され、ハロタンのような他の麻酔薬に置き換えられました。.
エーテルの精神
エタノールと混合したエーテルを使用して、胃の鼓腸およびより軽い形態の胃痛の治療に使用される、エーテルの精神と呼ばれる溶液を形成した。.
血行の評価
エーテルは腕と肺の間の血液循環を評価するために使用されてきました。エーテルは腕に注入され、血液を右心房、次に右心室に、そしてそこから肺に運びます。.
エーテルの注入から呼気中のエーテル臭の吸収までの経過時間は約4〜6秒です。.
教育ラボ
エーテルは多くの実験で実験室を教えるのに使われています。例えば、メンデルの遺伝学の法則のデモンストレーションでは.
エーテルは、ショウジョウバエ属のハエを麻痺させ、遺伝学の法則を証明するためにそれらの間の必要な交差を可能にするために使用されます。
参考文献
- Graham Solomons T.W.、Craig B. Fryhle。 (2011)。有機化学アミン(10番目 版。)。ワイリープラス.
- Carey F.(2008)。有機化学(第6版)。マックグローヒル.
- セビエ。 (2018)。ジエチルエーテルサイエンスダイレクト。以下から取得しました:sciencedirect.com
- ブリタニカ百科事典の編集者。 (2018)。エチルエーテルブリタニカncyclopædia。取得元:britannica.com
- PubChem(2018)。エーテル取得元:pubchem.ncbi.nlm.nih.gov
- ウィキペディア(2018)。ジエチルエーテル取得元:en.wikipedia.org
- 安全シートXI:エチルエーテル。 [PDF]以下から回復しました:quimica.unam.mx


