酸化銅の処方、性質、リスクと用途
の 酸化第二銅, 酸化銅(II)とも呼ばれ、式CuOの化合物です。その構造は図1に示されています(EMBL-EBI、2017)。.
酸化第二銅は、テノライトやパラマラコナイトなどの鉱物の成分の1つとして自然界に見られます。それはペルー、ボリビアなどの国々で、主に南アメリカの世界中の鉱物から抽出されます。.
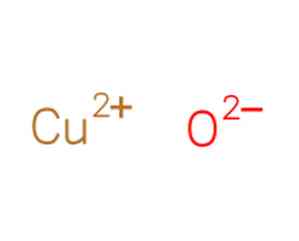
炭酸アンモニウムやアンモニアなどのいくつかの化合物はミネラルの抽出を促進するために使用されます.

酸化第二銅は主に鉱物中の抽出によって製造されますが、工業的に製造するためのいくつかのプロセスがあります。.
工業では、酸化第二銅は硝酸第二銅三水和物(100-20°C)、水酸化第二銅(100°C)または炭酸銅(250°C)の着火反応によって製造されます。
2Cu(NO3)2 →2CuO + 4NO2 + ○2
Cu(OH)2→CuO + H2O(l)
カッコウ3 →CuO + CO2
それはまた、銅金属を空気中で約800℃に加熱することによって合成的に調製される(酸化銅処方、S.F。)。.
酸化第二銅の物理的および化学的性質
酸化銅(II)イオン構造を持つ黒色の微粉末として表示されます。その外観は図3に示されています.

分子は、二価カチオン性銅Cu + 2とアニオン性酸素O-2によって形成されます。分子は単斜晶系を形成し、各銅原子は4つの酸素原子で配位しています。.
それは他の酸化銅:Cu 2 O酸化第一銅と密接に関連している(National Center for Biotechnology Information。、2005).
その分子量は79.545 g / mol、密度は6.315 g / mlです。融点は1326℃で、酸素を放出して分解し、沸点は2000℃以上です。.
この化合物は、水、アルコール、水酸化アンモニウム、炭酸アンモニウムに不溶であり、塩化アンモニウムおよびシアン化カリウムに可溶である(Royal Society of Chemistry、2015).
酸化銅は両性であるため、酸やアルカリ溶液に溶ける可能性があります。アルカリ性溶液中で、それは反応して他の銅塩を形成します。
2MetalOH + CuO + H2O→メタル2[Cu(OH)4]
酸性溶液中では、それはまた反応して他の銅塩を形成する。
CuO + 2HNO3 →Cu(NO3)2 + H2○
CuO + 2HCl→CuCl2 + H2○
アルミニウム、水素またはマグネシウムと接触して加熱すると爆発する。また、加熱すると有毒な蒸気が発生します。.
反応性と危険性
酸化銅(II)は経口摂取により非常に有毒で有毒です。中枢神経系および内分泌系に損傷を与える(AZoM、2013).
目や肌にも刺激があります。不燃性、安定かつ還元剤、硫化水素、アルミニウム、アルカリ金属、微粉末金属との相溶性がない(Fisher scientiffic、2009).
目に入った場合は、コンタクトレンズを装着しているかどうかを確認して、すぐに取り外してください。.
まぶたを開いたままにして、眼を流水で少なくとも15分間すすぐべきです。冷たい水を使うことができます。軟膏は目には使用しないでください.
化学物質が衣服と接触した場合は、自分の手と体を保護してできるだけ早くそれを取り除いてください。犠牲者を安全シャワーの下に置く.
手のような被害者の露出した皮膚に化学物質が蓄積した場合は、流水と研磨剤の入っていない石鹸で汚染された皮膚を優しく慎重に洗ってください。.
冷たい水を使うことができます。刺激が続く場合は、医師の診察を受けてください。再使用する前に汚染された衣類を洗う.
皮膚との接触が深刻な場合は、消毒石鹸で洗い、抗菌クリームで汚れた皮膚を覆ってください。.
吸入の場合、被害者は換気の良い場所で休憩することを許可されるべきです。吸入がひどい場合は、被害者をできるだけ早く安全な場所に避難させてください。.
シャツの襟、ベルト、ネクタイなどの衣類の締め付けを緩めます。被害者が呼吸が困難であると感じた場合は、酸素を投与する必要があります。.
犠牲者が呼吸していない場合は、口対口蘇生術が行われる。吸入した物質が有毒、感染性または腐食性である場合、口から口への蘇生を行うのを助ける人が危険をもたらす可能性があることを常に考慮に入れて.
摂取した場合、嘔吐を誘発しないでください。シャツの襟、ベルト、ネクタイなどの衣類の締め付けを緩めます。犠牲者が呼吸をしていない場合は、口対口蘇生を実施する.
すべての場合において、直ちに医師の診察を受けるべきです(化学物質安全データシート、酸化銅、2013年).
用途
酸化第二銅は、結晶、磁器エナメル、および人工宝石の顔料として使用されています。酸化物はそのような材料に青緑色がかった色合いを加える。.
石油ガスの脱硫剤、酸化触媒、電解電極にも使用されています(Encyclopaedia Britannica、2017)。.
酸化第二銅は、いくつかのプロセスで中間製品を製造するために化学および農薬業界で広く使用されています.
それは広く使用されている酸化/還元剤であり、特に石油の生産において、化学反応におけるプロセスの調整剤です。.
酸化第二銅は塗料や塗料を製造するのに使用され、またいくつかのエアーケア製品の成分です。.
動物の栄養補助食品としてはめったに使用されませんが、バンドギャップが狭いためp型半導体としての用途もあります。それはシロアリの酸化鉄の代替として使用されています.
その殺菌性および殺菌性のために、酸化銅(II)は殺虫剤および燻蒸剤としての用途もあります。.
それは主にジャガイモの植物の処理や船体の防汚剤として使用されています。防汚剤はボートの底のフジツボや他の有機体の形成を防ぐ材料です.
これらの生物が船の船体内で成長すると、船が水を通過するときに発生する摩擦を増大させ、その結果速度が低下します。.
この化合物は木材の防腐剤としても使用され、フェンスポスト、削りくず、デッキ、屋根ふき、帯状疱疹、海壁、その他の淡水および海洋構造物を昆虫や真菌から保護します。 (Thomson Gale、2006).
参考文献
- (2013年8月21日)。酸化銅(II)半導体azom.comから回復しました.
- 酸化銅フォーミュラ。 (S.F.)。 softschools.comから回復しました.
- EMBL-EBI (2017年2月2日)。酸化銅(II)。 ChEBI.ac.ukから取得.
- ブリタニカ百科事典(2017年5月16日)。銅(Cu) britannica.comから回収.
- フィッシャーの科学性(2009年9月20日)。製品安全データシート酸化銅(II)。 fke.uitm.edu.my.myから取得.
- 化学物質等安全データシート(2013年5月21日)。 sciencelab.comから回復しました.
- 国立バイオテクノロジー情報センター...(2005年3月26日)。 PubChem化合物データベース。 CID = 14829。 PubChemから取得.
- 化学の王立協会。 (2015)酸化銅(II) chemspider.comから取得.
- トムソンゲイル。 (2006)。酸化銅(II) encyclopedia.comから回収.


