酸化リチウムの配合、特性、リスクおよび用途
の 酸化リチウム 式Liの無機化合物です。2あるいは、リチウム金属が空気中で燃焼して酸素と結合すると、少量の過酸化リチウムと一緒に形成される.
1990年代まで、金属とリチウムの市場は鉱物鉱床からの米国の生産によって支配されていました、しかし21世紀の初めに生産のほとんどは米国以外の源から得られました。オーストラリア、チリ、ポルトガルは世界で最も重要な供給国でした。ボリビアは世界のリチウム鉱床の半分を持っています、しかしそれは大きな生産者ではありません.
最も重要な市販品は炭酸リチウムLi2CO3, 鉱物または塩水からいくつかの異なる方法で製造されたもの.
リチウムが空気中で燃焼すると、主生成物は酸化リチウムの白色酸化物、Li2さらに、いくらかの過酸化リチウムが生成され、Li2○2, また白.
水酸化リチウム、LiOH、または過酸化リチウム、Li 2 O 2の熱分解によっても可能です。
4Li + O2(g)→2Li2O(s)
2LiOH +熱→Li2O(s)+ H2O(g)
2Li2○2+熱→2Li2O(s)+ O2(g)
物理的および化学的性質
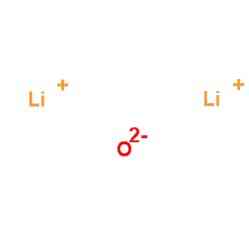
酸化リチウムは、香りや塩味がない、リチアとして知られる白い固体です。その外観は図2に示されています(国立バイオテクノロジー情報センター、2017年).

図2:酸化リチウムの外観
酸化リチウムは、塩化ナトリウム(面を中心とした立方体)のそれに類似したアンチフロライト幾何学を有する結晶である。その結晶構造を図3に示します(Mark Winter [The University of Sheffield and WebElements Ltd、2016]。.
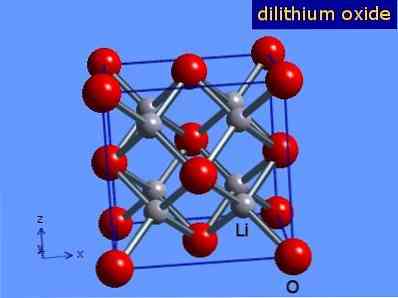
図3:酸化リチウムの結晶構造.
その分子量は29.88g / mol、その密度は2.013g / mL、そして融点および沸点はそれぞれ1438℃および2066℃である。この化合物は水、アルコール、エーテル、ピリジン、ニトロベンゼンに非常に溶けやすい(Royal Society of Chemistry、2015).
酸化リチウムは水蒸気と容易に反応して水酸化物を形成し、二酸化炭素と反応して炭酸塩を形成する。そのため、清潔で乾燥した雰囲気で保管および処理する必要があります。.
酸化物化合物は電気を発生させません。しかしながら、ペロブスカイトの特定の構造化酸化物は、固体酸化物型燃料電池および酸素発生システムのカソードに用途を見出す電子伝導体である。.
それらは少なくとも一つの酸素アニオンと一つの金属カチオンを含む化合物である(American Elements、S.F.)。.
反応性と危険性
酸化リチウムは、強酸、水、二酸化炭素とは相容れない安定な化合物です。我々の知る限りでは、酸化リチウムの化学的、物理的および毒物学的特性は調査されておらず、詳細に報告されていない。.
リチウム化合物の毒性は、それらの水への溶解度の関数です。リチウムイオンは中枢神経系に毒性があります。この化合物は、吸入または経口摂取したときに、眼、皮膚に接触すると非常に腐食性の刺激性がある(ESPI METALS、1993).
目に入った場合は、コンタクトレンズを着用しているかどうかを確認して、すぐに取り外してください。まぶたを開いたままにして、眼を流水で少なくとも15分間すすぐべきです。冷たい水を使うことができます。軟膏は目には使用しないでください.
化学物質が衣服と接触した場合は、自分の手と体を保護してできるだけ早くそれを取り除いてください。犠牲者を安全シャワーの下に置く.
手のような被害者の露出した皮膚に化学物質が蓄積した場合は、流水と研磨剤の入っていない石鹸で汚染された皮膚を優しく慎重に洗ってください。冷たい水を使うことができます。刺激が続く場合は、医師の診察を受けてください。再使用する前に汚染された衣類を洗う.
吸入の場合、被害者は換気の良い場所で休憩することを許可されるべきです。吸入がひどい場合は、被害者をできるだけ早く安全な場所に避難させてください。.
シャツの襟、ベルト、ネクタイなどの衣類の締め付けを緩めます。被害者が呼吸が困難であると感じた場合は、酸素を投与する必要があります。犠牲者が呼吸していない場合は、口対口蘇生術が行われる.
吸入した物質が有毒、感染性または腐食性である場合、口から口への蘇生を行うのを助ける人が危険をもたらす可能性があることを常に考慮に入れて.
すべての場合において、直ちに医師の診察を受けるべきです(SIGMA-ALDRICH、2010).
用途
酸化リチウムはセラミック釉薬のフラックスとして使用され、銅で青、コバルトで薔薇を作ります。酸化リチウムは水や水蒸気と反応して水酸化リチウムを形成するので、それらから分離する必要があります。.
酸化リチウム(Li2その高いトリチウムポテンシャルを有するO)は、その高密度のリチウム原子(他のリチウムまたは金属リチウムセラミックと比較して)およびその導電性のために、DT核融合発電所の固体培養材料の魅力的な候補である。比較的高い熱(酸化リチウム(Li 2 O)、SF).
李2あるいは、核融合ブランケットの運転中に中性子照射下で高温にさらされます。これらの状況下では、Li中に多数の照射欠陥が生じる。2あるいは、ヘリウム誘起膨潤、比較的高い熱膨張、粒子成長、低温でのLiOH(T)形成および析出、ならびに高温でのLiOH(T)質量の輸送など。.
また、Li2あるいは、Li間の熱膨張の違いから生じるストレスを受けることになります。2Oおよび構造材料Liのこれらの特性2あるいはそれらは、ブランケットの製造と設計の両方において困難な工学的問題を引き起こす。.
考えられる新しい用途は、携帯電話からラップトップや電池式自動車に電子機器に電力を供給するために使用されるリチウムイオン電池のカソードとしてのコバルトと酸化リチウムの代替品としてです(Reade International Corp、2016)。.
参考文献
- マーク・ウィンター[シェフィールド大学ウェブエレメンツ社(2016)]. webelements. リチウムから撮影:酸化リチウムリチウムwebelements.com.
- アメリカの要素(S.F.). 酸化リチウム. americanelementsから取得しましたamericanelements.com.
- ESPIメタル(1993年6月). 酸化リチウム. espimetalsからの撮影espimetals.com.
- 酸化リチウム(Li 2 O). (S.F.)。 ferp.ucsd.eduから取得したferp.ucsd.edu.
- 国立バイオテクノロジー情報センター(2017年6月24日). PubChem化合物データベース。 CID = 166630. PubChemから取得されたpubchem.ncbi.nlm.nih.gov.
- Reade International Corp.(2016). 酸化リチウム粉末(Li 2 O). reade reade.comから撮った
- 化学の王立協会。 (2015年). 酸化リチウム.chemspiderchemspider.comから取得しました.
- シグマアルドリッチ。 (2010年). 化学物質等安全データシート酸化リチウム. chemblinkから取得しましたchemblink.com.


