酸化マンガン(MnO 2)の化学構造、性質および用途
の 酸化マンガン (MnO2)は、酸化数+4の元素マンガンと酸素とによって形成される無機化合物であり、酸化物の形成において、酸化数−2を有する。それはまた酸化マンガン(IV)および無水マンガンの名前で知られています.
ダークコーヒーからブラックコーヒーまでしっかりしています。それは、鉱物のピロルサイト、黒色および結晶化した形成樹状突起(分岐伸長)として天然に存在する。過マンガン酸カリウムの酸化作用によるグリコールの形成後、エチレンと過マンガン酸カリウムとの間の反応における黒色残渣として得ることができる。.

それは酸化剤のその特性のためにガラス産業において非常に重要です、それはそれが鉄化合物から来る緑色を除去して、それらを鉄に変換するからです。.
索引
- 1化学構造
- 2プロパティ
- 3つの用途
- 3.1触媒として
- 4健康への影響
- 5参考文献
化学構造
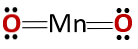
この化合物の化学構造は、金属と非金属からなるために予想されるように、無水物の化学構造に対応し、塩基性酸化物のそれには対応しない。.
この特別なケースは、それが持っているさまざまな酸化状態でマンガンによって仮定された挙動によるものです。したがって、酸化状態+ 2および+ 3では、酸化物MnOおよびMnが形成されます。2○3 それぞれ、水と反応すると、それらはそれぞれ水酸化マンガンと水酸化マンガンを形成する。.
ただし、Mn2○3 弱酸性媒体では、無水物のように振舞います。酸化状態が+ 4、+ 6、+ 7の場合、MnOは2, MnO3 とMnO4 水と反応すると酸を形成する.
わずかに酸性の媒体ではMnO2 それは塩基性酸化物のように振る舞うので、それは対応する水酸化物を形成することができる.
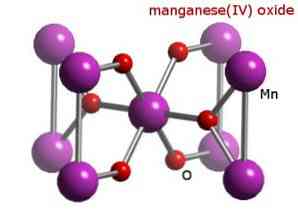

この場合、化合物が酸または塩基として振る舞うことができるという両性の性質については言及されていないことに留意しなければならない。これはMnの挙動の特別な場合です.
プロパティ
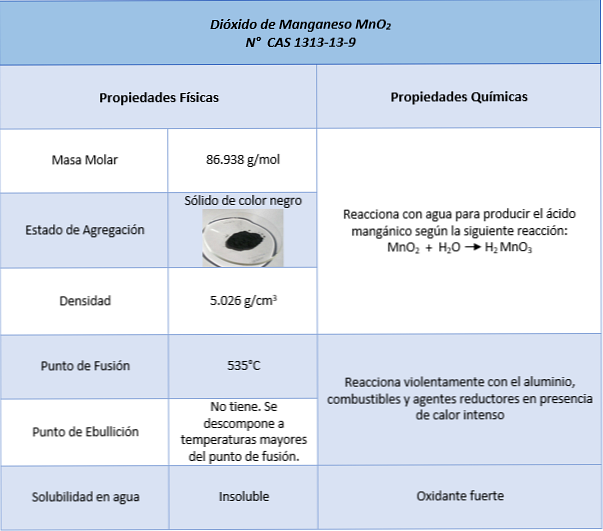
用途
- それはマンガンの源として使用されています
- アルカリ電池の酸化剤として
- ガラス、セラミックス、磁器用塗料.
- 塩素とヨウ素を得るには.
- 酸素ガスと水の生成のための過酸化水素の分解.
- 酸素ガスと塩化カリウムの製造のための塩素酸カリウムの分解反応.
- アセトンまたはジクロロメタンに溶解し、一級アルコールをアルデヒドに、二次ケトンに酸化する.
- アルカリ電池の製造.
触媒として
これは、Hなどの硫化物の除去のための酸化物還元反応に適用される。2SやFeのような陽イオン+2 とMn+2 , このタイプの化合物によって汚染されている地下水に含まれるヒ素やラジオ.
この汚染は、有害物質の管理されていない投棄、汚染された土壌の洗浄、または水の抽出時に化学元素が存在することによって発生する可能性があります。.
MnO2 フィルターとして使用されるパイロサイトから得られる高純度(Filox)は地下水からこの種の不純物を除去するための最も効果的な手段です。.
健康への影響
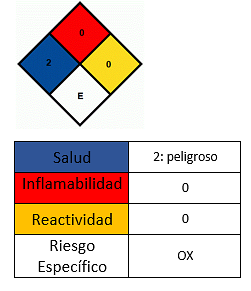
- 皮膚との接触を避ける.
- 接触した場合は、対応する部分を洗ってください。.
- 粉末を吸い込まないでください.
- 目に入ったときに刺激と発赤が見られることがあります。多量の水で洗い流し、目に入ったところに水を流して重症の場合には医療支援を受ける。.
- 皮膚に接触すると刺激および発赤が観察される。患部を多量の水と石鹸で洗う.
- 長時間の皮膚接触はあなたの天然脂肪を取り除き、皮膚炎を引き起こします.
- 吸入するとインフルエンザのような状態(金属性のフューム)を引き起こすことがあります。その状態は、高熱、悪寒、口渇および喉の痛み、筋肉痛および頭痛を特徴とする。.
- 気道を刺激し、呼吸器感染症(肺炎)の発生率を高める可能性があります。肺を通した無機マンガン塩の吸収による中毒はありそうもないですが、慢性の中毒は起こることができます.
- 二酸化マンガンからの粉塵やヒュームへの長期の長期暴露は中枢神経系に影響を及ぼし、パーキンソン病の発症、歩行困難、筋肉のけいれんおよび行動の変化につながる可能性があります。.
- 経口摂取は腹痛や吐き気を引き起こす可能性があります.
- それは可燃性ではありません、しかしそれは白熱材料で火を広げるのを助けます。 535℃を超える温度に加熱すると、物質は酸化マンガン(III)に分解する。2○3 可燃性であり、火災の危険性が高まります。この場合火は泡か二酸化炭素と消火するべきです.
- こぼれた場合は、適切な個人保護なしで化合物を操作しないでください。.
- 化合物を密閉された容器に入れ、冷たい乾燥した場所に、有機物や可燃物などの不適合な物質から離して保管する.
- 保管場所は乾燥していて、酸による腐食に強く、排水性に優れた床が必要です。.
- 手袋、安全ゴーグル、防湿マスク、ほこりや煙などの個人用保護具を使用する必要があります。.
参考文献
- B、(2015)、二酸化マンガン、英国王立化学会 - 化学界
- Karal、(2014年)、二酸化マングネソ、安全データシート、回収、karal.com.mx
- あなたのバーチャル先生(2015-02-25)無機マンガン化合物(特別な場合1) - 理論上のレッスン)、youtube.comから取得
- Ecured、(s.f)、二酸化マンガン、ecured.cuから回収
- Angarita G、ジョニー、(2017)、二酸化マンガン:優れた技術. ハイドロテック, hydrotecocr.comから回復した
- Fernández、G.、(2015)、二酸化マンガンマンガン2/アセトン, 有機化学, quimicaorganica.netから回復しました
- Tronox、(2011)、二酸化マンガン、安全データシート、回収、tronox.com


