酸化銀(Ag 2 O)の構造、性質、命名法および用途
の 酸化銀 化学式がAgの無機化合物です。2O.その原子を結合する力は完全にイオン性です。それゆえ、それは2つのAgカチオンの比率があるイオン性固体からなる。+ 陰イオンOと静電的に相互作用する2-.
酸化物アニオン、O2-, それは表面の銀原子と環境の酸素との相互作用から生じる。鉄や他の多くの金属と非常によく似た方法で。赤くなり錆びるのではなく、銀色の小片や宝石が黒くなり、酸化銀の特徴.

たとえば、上の画像ではさびた銀の杯が見えます。表面が黒くなっていることに注目してください。だからこそ、さびた銀色の物体でさえ装飾的用途には十分魅力的であると考えることができるのです。.
酸化銀の特性は、一見すると元の金属表面を損なわないようなものである。それは空気中の酸素との単純な接触によって室温で形成される。さらに興味深いことに、高温(200℃以上)で分解する可能性があります。.
これは、画像のガラスが保持されていて、強い炎の熱が加えられると、銀色の光沢が回復することを意味します。したがって、その形成は熱力学的に可逆的なプロセスです。.
酸化銀も他の特性を持ち、その単純なAg式を超えて2あるいは、それは複雑な構造組織と豊富な種類の固体を含みます。しかし、Ag2それとも、Agの横にあるのでしょうか。2○3, 銀の酸化物の最も代表的なもの.
索引
- 1酸化銀の構造
- 1.1バレンシア数による変化
- 2物理的および化学的性質
- 2.1分子量
- 2.2外観
- 2.3密度
- 2.4融点
- 2.5 Kps
- 2.6溶解度
- 2.7共有文字
- 2.8分解
- 3命名法
- 3.1バレンシアⅠとⅢ
- 3.2複雑な酸化銀の体系的な命名法
- 4つの用途
- 5参考文献
酸化銀の構造
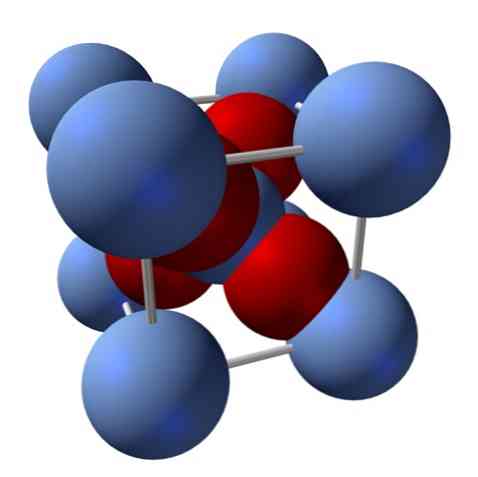
その構造はどうですか?冒頭で述べたように、それはイオン性の固体です。このため、その構造中に共有結合Ag-OもAg = Oも存在し得ない。もしあれば、この酸化物の性質は劇的に変化するでしょう。それはAgイオンです+ とO2- 2:1の比率で静電引力を経験する.
酸化銀の構造は、結果として、イオン力が銀イオンを空間に放出する方法によって決定される。+ とO2-.
たとえば、上の図では、立方晶系の単位格子があります。+ 銀色の青い球とO2- 赤みを帯びた球.
球の数を数えると、一見したところ、9つの銀色の青と4つの赤い色があることがわかります。ただし、立方体内に含まれている球の断片だけが考慮されます。これらの数を数えることは、全球体のほんの一部であり、Agの2:1の比率が満たされなければなりません。2○.
AgO四面体の繰り返し構造4 他の4つのAgに囲まれて+, すべての黒いソリッドが構築されています(これらの結晶配列が持つことができるギャップまたは不規則性を取り除きます).
バレンシア数による変化
AgO四面体には焦点を当てない4 線AgOAg(上の立方体の頂点を観察)では、別の観点から見ると、酸化銀固体は(傾斜しているが)直線的に配置された複数のイオン層からなることになる。 Agの周りの「分子」幾何学の結果としてこれらすべて+.
上記は、そのイオン構造のいくつかの研究によって裏付けられている.
銀は、電子を失うとその電子配置が[Kr] 4 dとなるので、主に価数+1で働く。10年, これは非常に安定しています。 Agなどの他の原子価2+ と銀3+ それらはほぼ完全に満たされた軌道から電子を失うのでそれらは不安定です.
Agイオン3+, しかしながら、それはAgと比較して比較的不安定ではない。2+. 実際には、それはAgの会社で共存することができます+ 構造を化学的に強化する.
その電子構成は[Kr] 4dです8, いくつかの安定性を与えるような方法で不対電子と.
Agイオンの周りの線形形状とは異なり+, それはAgイオンのそれであることがわかった3+ スクエアフラットです。したがって、銀イオンを含む酸化銀3+ AgOの正方形からなる層で構成されます4 (四面体ではない)AgOAg線によって静電的に結合されている。これはAgの場合です4○4 Ag2O∙Ag2○3 単斜晶系構造を有する.
物理的および化学的性質

メイン画像の銀色のカップの表面に傷を付けると、ベタ塗りになります。これは、黒だけでなく、茶色または茶色の色調もあります(上の画像)。現時点で報告されているその物理的および化学的性質のいくつかは以下の通りです。
分子量
231,735 g / mol
外観
粉末状の黒褐色固体(イオン性固体であるにもかかわらず、それは結晶質の外観を欠いていることに注意されたい)。それは無臭であり、水と混合されたそれはそれに金属味を与える
密度
7.14 g / mL.
融点
277〜300℃。確かに、それは銀に固く溶けます。すなわち、それはおそらく液体酸化物を形成する前に分解する.
Kps
1.52∙10-8 20℃の水中で。それゆえ、それは水にほとんど溶けない化合物です。.
溶解度
その構造のイメージを注意深く見ると、Agの球が2+ とO2- 彼らはほとんどサイズが合わない。結果として、小さな分子だけが結晶格子の内部に浸透することができ、ほとんどすべての溶媒に不溶になります。塩基や酸など、反応するものを除く.
共有文字
酸化銀はイオン性化合物であると繰り返し言われてきたが、その低い融点のようなある種の性質はこの記述と矛盾する。.
確かに、共有結合特性を考慮しても、その構造について説明されている内容は崩れません。それをAgの構造に追加すれば十分です。2共有結合を示す球と棒のモデル.
また、四面体と正方形の平面AgO4, AgOAg線と同様に、それらは共有(または共有イオン)結合によって結合されるであろう。.
これを念頭に置いて、Ag2それとも実際にはポリマーになります。しかしながら、それを共有結合性を有するイオン性固体と見なすことが推奨されている(そのリンクの性質は今もなお挑戦である)。.
分解
最初に、その形成は熱力学的に可逆的であると述べられたので、それは熱を吸収してその金属状態に戻る。これらすべては、このような反応に対する2つの化学式で表すことができます。
4Ag + O2(g)=> 2Ag2O(s)+ Q
2Ag2O(s)+ Q => 4Ag(s)+ O2(g)
ここで、Qは式の熱を表します。錆びた銀の杯の表面を燃やす火が銀色の輝きを戻す理由.
したがって、Agがあると仮定することは困難です。2O(l)それは熱によって即座に分解するから。そうでなければ、圧力が高すぎて前記褐色黒色液体を得ることができない。.
命名法
Agイオンの可能性が導入されたとき2+ と銀3+ 一般的で優勢なAg以外に+, 「酸化銀」という用語は、Agを指すには不十分であるように見え始めます。2○.
これはAgイオンが+ 他よりも豊富なので、Agが撮影されます2あるいは唯一の酸化物として。まったく正しくない.
あなたがAgを考えるなら2+ その不安定性を考えると実質的に存在しないので、価数+1と+3のイオンだけが存在することになる。すなわち、Ag(I)とAg(III).
バレンシアⅠとⅢ
Ag(I)が最小の原子価であるため、名前に接尾辞-osoを追加して命名されています。 銀河. だから、Ag2あるいは、それは:酸化アルジェントソ、または体系的な命名法によれば、一酸化二プラタである。.
Ag(III)が完全に無視される場合、その伝統的な命名法は次のようになります。酸化アルゼンチンの代わりに酸化銀.
一方、より大きい価数であるAg(III)は、その名前に接尾辞-icoが追加されています。だから、Ag2○3 :酸化銀(2 Agイオン)3+ 3つのOを使って2-)また、体系的な命名法によると、その名前は次のようになります。.
Agの構造が見られたら2○3, それは、オゾンによる酸化の産物であると推定することができます。3, 酸素の代わりに。それゆえ、その共有結合性は、Ag-O-O-O-AgまたはAg-O結合を有する共有結合性化合物であるので、より大きくなければならない。3-Ag.
複合酸化銀の体系的な命名法
AgO、Agとも呼ばれる4○4 Ag2O∙Ag2○3, それは+1価と+3価の両方を有するので、それは酸化銀(I、III)である。体系的な命名法によると、その名前は次のようになります。.
この命名法は、他の化学量論的により複雑な酸化銀に関しては非常に役立ちます。たとえば、2つのソリッド2Agを考えます。2O∙Ag2○3 と銀2O∙3Ag2○3.
最初のものをもっと適切な方法で書くと、次のようになります。Ag6○5 (AgとOの原子を数えて加えます)。そのとき彼の名前は五酸化ヘキサプレートになるでしょう。この酸化物はAgよりも銀の組成が少ないことに留意されたい。2O(6:5 < 2:1).
そうでなければ2番目のソリッドを書いている間、それは次のようになります。Ag8○10年. その名前は八酸化物デカオキシド(8:10または4:5の比を有する)であろう。この仮想の酸化銀は「非常に酸化されている」でしょう.
用途
酸化銀の新しい洗練された用途を探し求める研究は今日もなお行われている。その用途のいくつかを以下に示します。
-それはアンモニア、硝酸アンモニウムおよび水に溶解されてTollens試薬を形成する。この試薬は、有機化学実験室における定性分析に役立つツールです。それは、試料中のアルデヒドの存在を決定することを可能にし、肯定的な応答は試験管内の「銀鏡」の形成である。.
-それは金属亜鉛と共に銀の酸化亜鉛の一次電池を形成する。これはおそらくその最も一般的で家庭的な用途の1つです。.
-それは例えばCOを吸収するガス精製器として役立つ。2. 温められると、閉じ込められたガスを放出し、数回再利用することができます.
-銀の抗菌特性のために、その酸化物は生物分析と土壌浄化の研究に役立ちます.
-それはアルデヒドをカルボン酸に酸化することができる温和な酸化剤です。それはまたホフマン反応(第三級アミン)にも使用されそして試薬または触媒として他の有機反応に参加する。.
参考文献
- Bergstresser M.(2018)。酸化銀処方、分解および生成勉強します。取得元:study.com
- 巻III / 17E-17F-41Cの執筆者および編集者。 (S.F.)。酸化銀(Ag(x)O(y))の結晶構造、格子定数(科学技術における数値データと機能的関係)、41C。スプリンガー、ベルリン、ハイデルベルク.
- Mahendra Kumar Trivedi、Rama Mohan Tallapragada、Alice Branton、Dahryn Trivedi、Gopal Nayak、Omprakash Latiyal、Snehasis Jana。 (2015)酸化銀粉末の物理的および熱的性質に及ぼすバイオフィールドエネルギー処理の潜在的影響バイオメディカルサイエンスとエンジニアリングの国際ジャーナル。 3巻、5号、pp。 62-68。土井:10.11648 / j.ijbse.20150305.11
- Sullivan R.(2012)。酸化銀の分解オレゴン大学取得元:chemdemos.uoregon.edu
- フリント、デヤンダ。 (2014年4月24日)酸化銀電池の用途偵察しています。取得元:sciencing.com
- Salman Montasir E.(2016)。紫外可視分光光度計を用いた酸化銀(Ag 2 O)のいくつかの光学的性質の研究[PDF]以下から取得しました:iosrjournals.org
- Bard Allen J.(1985)。水溶液中の標準電位マルセルデッカー。取得元:books.google.co.ve


