窒素酸化物(NOx)の異なる配合と命名法
の 窒素酸化物 それらは本質的に窒素と酸素原子の間の結合を含む気体の無機化合物です。そのグループの化学式はNOです×, 酸化物が異なる割合の酸素と窒素を有することを示す.
窒素は周期表の15族を、酸素は16族をリードしています。両方の元素は、期間2のメンバーです。この近さが、N-O結合が酸化物中で共有結合である理由です。このように、窒素酸化物中の結合は共有結合である.
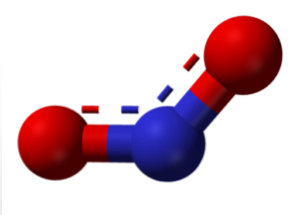
これらすべての関連は分子軌道の理論を使って説明することができ、それはこれらの化合物のいくつかの常磁性(最後の分子軌道では不対電子)を明らかにする。これらのうち、最も一般的な化合物は一酸化窒素と二酸化窒素です。.
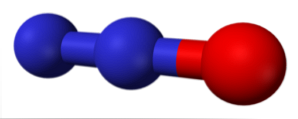
上の画像の分子は二酸化窒素(NO)の気相における角構造に対応します2)対照的に、一酸化窒素(NO)は線状構造を有する(両方の原子に対するsp混成を考慮して).
窒素酸化物は、自動車の運転やタバコの喫煙から、汚染廃棄物としての産業プロセスまで、多くの人間の活動によって生成されるガスです。しかし、NOは雷雨の中で酵素反応と稲妻によって自然に生成されます。N2(g)+ O2(g)=> 2NO(g)
光線の高温は、この反応が通常の条件下で起こるのを防ぐエネルギー障壁を壊します。どんなエネルギー障壁?それは三重結合N≡Nによって形成され、N分子を作る2 大気からの不活性ガス.
索引
- 1酸化物中の窒素と酸素の酸化数
- 2異なる定式化と命名法
- 2.1亜酸化窒素(N2O)
- 2.2一酸化窒素(NO)
- 2.3三酸化窒素(N 2 O 3)
- 2.4二酸化窒素と四酸化窒素(NO 2、N 2 O 4)
- 2.5五酸化二窒素(N 2 O 5)
- 3参考文献
酸化物中の窒素と酸素の酸化数
酸素の電子配置は[He] 2sです22p4, その原子価殻のオクテットを完成するために2つの電子だけを必要とする。つまり、2つの電子を獲得し、-2に等しい酸化数を持つことができます。.
一方、窒素の電子配置は[He] 2sです。22p3, その原子価オクテットを埋めるために3個までの電子を得ることができる。例えば、アンモニア(NH)の場合3)は−3に等しい酸化数を有する。しかし、酸素は水素よりはるかに電気陰性度が高く、窒素にその電子を共有させることを強制します。.
窒素は酸素と共有できる電子の数はいくつですか。原子価殻の電子を一つずつ共有すると、酸化数+5に対応して、5つの電子の限界に達します。.
したがって、酸素との結合数に応じて、窒素の酸化数は+ 1から+ 5の間で変化します。.
異なる処方と命名法
窒素酸化数の昇順で、窒素酸化物は次のとおりです。
- N2または、亜酸化窒素(+1)
- NO、一酸化窒素(+2)
- N2○3, 三酸化二窒素(+3)
- いいえ2, 二酸化窒素(+4)
- N2○5, 五酸化二窒素(+5)
亜酸化窒素(N2O)
亜酸化窒素(または笑気として一般的に知られている)は、わずかに甘い香りと反応性がほとんどない無色のガスです。それはN分子として可視化することができます2 一方の端に酸素原子を追加した(青い球)。それは硝酸塩の熱分解によって準備され、麻酔薬および鎮痛剤として使用されます.
窒素はこの酸化物中で+1の酸化数を有し、それはそれがあまり酸化されておらずそして電子に対するその要求が説得力がないことを意味する。ただし、安定した分子窒素になるには、2つの電子(各窒素に1つずつ)を取得するだけで済みます。.
塩基性および酸性溶液での反応は次のとおりです。
N2O(g)+ 2H+(ac)+ 2e- => N2(g)+ H2O(l)
N2O(g)+ H2O(l)+ 2e- => N2(g)+ 2OH-(ac)
これらの反応は、熱力学的には安定な分子Nの形成によって支持されている。2, ゆっくり起こり、電子対を供与する試薬は非常に強い還元剤でなければならない.
一酸化窒素(NO)
この酸化物は無色の反応性常磁性ガスからなる。亜酸化窒素と同様に、それは線状分子構造を有するが、N = O結合が三重結合特性も有するという大きな違いがある。.
NOは空気中で急速に酸化されてNOを生成する。2, そしてより酸化された窒素原子(+4)を持つより安定な分子軌道を生成する.
2NO(g)+ O2(g)=> 2NO2(g)
生化学的および生理学的研究は、生物におけるこの酸化物の良性の役割の背後にあります.
分子軌道中の不対電子の非局在化のために(その高い電気陰性度のために)それは酸素原子の方へ向けられるので、それは他のNO分子とN − N結合を形成することができない。反対のことがNOで起こる2, それは気体二量体を形成することができる.
三酸化窒素(N2○3)
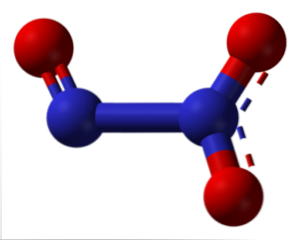
構造の点線は二重結合の共鳴を示す。すべての原子のように、それらはsp混成を持っています2, 分子は平らで、分子間相互作用は三酸化窒素が-101℃以下の青い固体として存在するのに十分効果的です。より高い温度でそれは溶けてNOとNOに解離する。2.
なぜそれは解離しているのですか?酸化数+2および+4は+3よりも安定しているので、後者は2つの窒素原子のそれぞれについて酸化物中に存在する。これもまた、不均衡から生じる分子軌道の安定性によって説明することができる。.
画像では、Nの左側2○3 NOの右側がNOに対応します。2. 論理的には、それは非常に低い温度(-20ºC)で以前の酸化物の合体によって作り出されます。 N2○3 亜硝酸無水物(HNO2).
二酸化窒素と四酸化窒素(NO)2, N2○4)
いいえ2 それは褐色または褐色の気体で、反応性で常磁性です。それは不対電子を有するので、それは他のNO気体分子と二量体化(結合)する。2 四酸化二窒素、無色のガスを形成するために、両方の化学種間のバランスを確立する:
2NO2(g) <=> N2○4(g)
それは有毒で多用途の酸化剤であり、イオン(オキソアニオン)中でのその酸化還元反応において不均化することができる。2- そしてNO3- (酸性雨が発生)またはNO.
同様に、NO2 オゾン濃度の変動を引き起こす複雑な大気中の反応に関与している3)地上レベルおよび成層圏.
五酸化二窒素(N2○5)
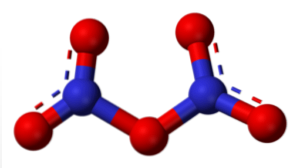
水和すると、それはHNOを生成します3, そしてより高濃度の酸では、酸素は主として部分正電荷−Oでプロトン化される。+-H、酸化還元反応を加速する
参考文献
- 尋ねる。 ((2006-2018)). 質問者. 2018年3月29日、askIITiansから取得:askiitians.com
- 百科事典Britannica、Inc.(2018). ブリタニカ百科事典. 2018年3月29日、ブリタニカ百科事典より検索:britannica.com
- トックスタウン。 (2017). トックスタウン. 2018年3月29日、Tox Townから取得:toxtown.nlm.nih.gov
- パトリシア・シャプリー教授。 (2010)。大気中の窒素酸化物イリノイ大学2018年3月29日、butane.chem.uiuc.eduから取得
- シヴァー&アトキンス。 (2008)。無機化学で グループ15の元素. (第4版、361〜366頁)。マックグローヒル