有機塩の物理化学的性質、用途および例
の 有機塩 それらは無数の特性を持つイオン化合物の密集した数です。それらは、それが電荷のキャリアになることを可能にする変換を受けた有機化合物から以前に由来し、そしてまた、その化学的同一性は関連するイオンに依存する。.
下の画像では、有機塩の2つの非常に一般的な化学式が示されています。 1つ目のR-AXは、その炭素構造内に原子またはA基が正電荷+または負電荷( - )を持つ化合物と解釈されます。.
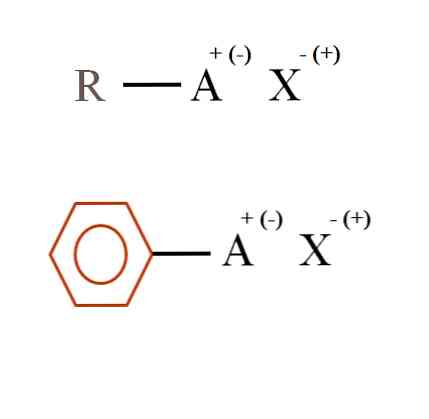
見てわかるように、RとAの間に共有結合R-Aがありますが、AはXイオンを引き付ける(またははじく)形式電荷を持っています。.
もしAが正であれば、それは何個のXと相互作用できますか? 1つだけで、電気的中性の原理を考えると(+ 1-1 = 0)。しかし、Xのアイデンティティは何ですか?アニオンXはCOであり得る。32-, 2つのカチオンを必要とするRA+;ハロゲン化物:F-, Cl-, Br-, などさらには別のRA化合物-. オプションは計り知れません.
また、有機塩は、茶色のベンゼン環に示されているような芳香族性を有することができる。安息香酸銅塩(II)、(C)6H5COO)2例えば、Cuは、Cuカチオンと相互作用する、負に荷電したカルボキシル基を有する2つの芳香族環からなる。2+.
索引
- 1物理的および化学的性質
- 1.1高分子量
- 1.2両親媒性物質と界面活性剤
- 1.3高沸点または融点
- 1.4酸度と塩基度
- 2つの用途
- 3有機塩の例
- 3.1カルボキシレート
- 3.2リチウムジアクリレート
- 3.3スルホニウム塩
- 3.4オキソニウム塩
- 3.5アミン塩
- 3.6ジアゾニウム塩
- 4参考文献
物理的および化学的性質
画像から、有機塩は3つの成分:有機、RまたはAr(芳香環)、イオン電荷Aを有する原子または基、および対イオンXからなると言える。.
化学的同一性および構造がそのような成分によって定義されるように、それらの特性はそれらに依存する.
この事実から、これらの塩の大部分を満たすある種の一般的性質をまとめることができます。.
高分子量
一価または多価の無機Xアニオンを仮定すると、有機塩は通常、無機塩よりもはるかに大きい分子量を有する。これは主に、その単純なC-C結合とそれらの水素原子が化合物に多くの質量を与える炭素骨格によるものです。.
それ故、それらはそれらの高分子量の原因であるRまたはArである。.
両親媒性物質と界面活性剤
有機塩は両親媒性化合物であり、すなわち、それらの構造は親水性末端と疎水性末端の両方を有する。.
そのような極値は何ですか? CまたはH原子は水分子に対して大きな親和性を持たないため、RまたはArは疎水性末端を表します。.
A+( - ), 電荷を持つ原子または基は親水性末端です。なぜなら、それは双極子モーメントに寄与し、水形成双極子(RA)と相互作用するからです。+ OH2).
親水性領域と疎水性領域が分極されると、両親媒性塩は界面活性剤となり、洗剤の製造に広く使用されています。 抗乳化剤.
高沸点または融点
無機塩と同様に、有機塩も液相または固相で支配する静電力のために高い融点および沸点を有する。.
しかし、有機成分RまたはArを持ち、静電気と一定の方法で競合する他のタイプのファンデルワールス力(ロンドン力、双極子 - 双極子、水素ブリッジ).
このため、有機塩の固体または液体構造は、第一に、より複雑で多様である。そのうちのいくつかは以下のように振る舞うことさえできます。 液晶.
酸度と塩基度
有機塩は通常、無機塩よりも強い酸または塩基である。これは、例えばアミン塩中のAが、追加の水素との結合のために正電荷を有するからである。+-H.次に、塩基と接触して、中性化合物に戻るためにプロトンを供与する。
RA+H + B => RA + HB
HはAに属しますが、中和反応に干渉するように書かれています.
一方、RA+ それは、ヒドロキシルアニオンまたはヒドロキシルOHに対して十分に安定な結晶ネットワークを有する固体を形成することができない、大きな分子であり得る。-.
この場合、塩RA+OH- それは強い基盤のように振る舞います。 NaOHやKOHと同じくらい塩基性でも:
RA+OH- + HCl => RACl + H2○
化学式の中でClアニオンが- それはOHを取り替える-, 塩RAを形成する+Cl-.
用途
有機塩の使用は、R、Ar、AおよびXの種類によって変わる。さらに、それらが向けられる用途は、それらが形成する固体または液体の種類にも依存する。これに関する一般性は次のとおりです。
-それらは他の有機化合物を合成するための試薬として役立つ。 RAXは、R 2の「供与体」として作用し、別の化合物に付加されて、優れた外向きの基を置き換えます。.
-それらは界面活性剤であるので、それらは潤滑剤としても使用できる。カルボン酸塩の金属塩がこの目的に使用される。.
-それらは広範囲の染料を合成することを可能にする。.
有機塩の例
カルボキシレート
カルボン酸は中和反応において水酸化物と反応し、カルボン酸塩を生じる。- M+;どこM+ それはどんな金属カチオン(Na+, Pb2+, K+, など)またはNHアンモニウムカチオン4+.
脂肪酸は長鎖脂肪族カルボン酸であり、それらは飽和でも不飽和でもよい。パルミチン酸(CH)は飽和3(CH2)14年COOH)。これはパルミチン酸塩、ステアリン酸(CH3(CH2)16COOHはステアリン酸塩を形成する。石鹸はこれらの塩で構成されています.
安息香酸の場合、C6H5COOH(ここでC6H5- それがベンゼン環である場合、それが塩基と反応すると安息香酸塩を形成する。すべてのカルボキシレートにおいて、-COO基- Aを表します(RAX).
リチウム二酢酸
二銅酸リチウムは有機合成に有用である。その式は[R-Cu-R]です。-李+, 銅原子は負電荷を帯びています。ここで、銅は画像の原子Aを表します.
スルホニウム塩
それらは有機硫化物とハロゲン化アルキルとの反応から形成される。
R2S + R'X => R2R'S+X
これらの塩では、硫黄原子は正の形式電荷(S+)3つの共有結合を有する.
オキソニウム塩
また、エーテル(スルフィドの酸素化類似体)はヒドロシドと反応してオキソニウム塩を形成する。
ROR '+ HBr <=> RO+HR '+ Br-
HBrの酸性プロトンはエーテルの酸素原子に共有結合している(R2○+-H)、積極的にそれをロードする.
アミン塩
アミンは、一級、二級、三級または四級、ならびにそれらの塩であり得る。それらの全ては、窒素原子に結合したH原子を有することを特徴とする。.
だから、RNH3+X- それは一級アミン塩です。 R2NH2+X-, 二級アミン。 R3NH+X-, 三級アミン。とR4N+X-, 四級アミン(四級アンモニウム塩)の合成.
ジアゾニウム塩
最後に、ジアゾニウム塩(RN2+X-またはarildiazonium(ArN)2+X-)、多くの有機化合物、特にアゾ染料の出発点を表す.
参考文献
- フランシスA.キャリー。有機化学(第6版、604〜605頁、697〜698頁、924頁)。マックグローヒル.
- Graham Solomons T.W.、Craig B. Fryhle。有機化学アミン(第10版)。ワイリープラス.
- ウィキペディア(2018)。塩(化学)撮影元:en.wikipedia.org
- スティーブンA.ハーディンガー。 (2017)図解有機化学用語集:塩。取得元:chem.ucla.edu
- シェブロンオロナイト。 (2011)。カルボキシレート[PDF]取得元:oronite.com


